PASSMED公式LINEの登録者特典|当サイトに掲載している図表の元データ&学習支援AI 薬科GPTをプレゼント♪
2024年5月22日、新薬18製品が薬価収載されました!
今回は、レケンビ(レカネマブ)の投与可否を判断するアミロイドβのPET検査薬である2製品(ビザミル静注とアミヴィッド静注)が薬価収載されました。
これまで、同検査薬は診療報酬の技術料の中で保険償還(PET:7,500点、PET/CT:8,625点)されていましたが、2024年6月から施行される診療報酬改定において、ビザミルやアミヴィッドを用いたPET検査の診療報酬が、薬剤料とPET検査の撮影等に係る技術料に分離されます。

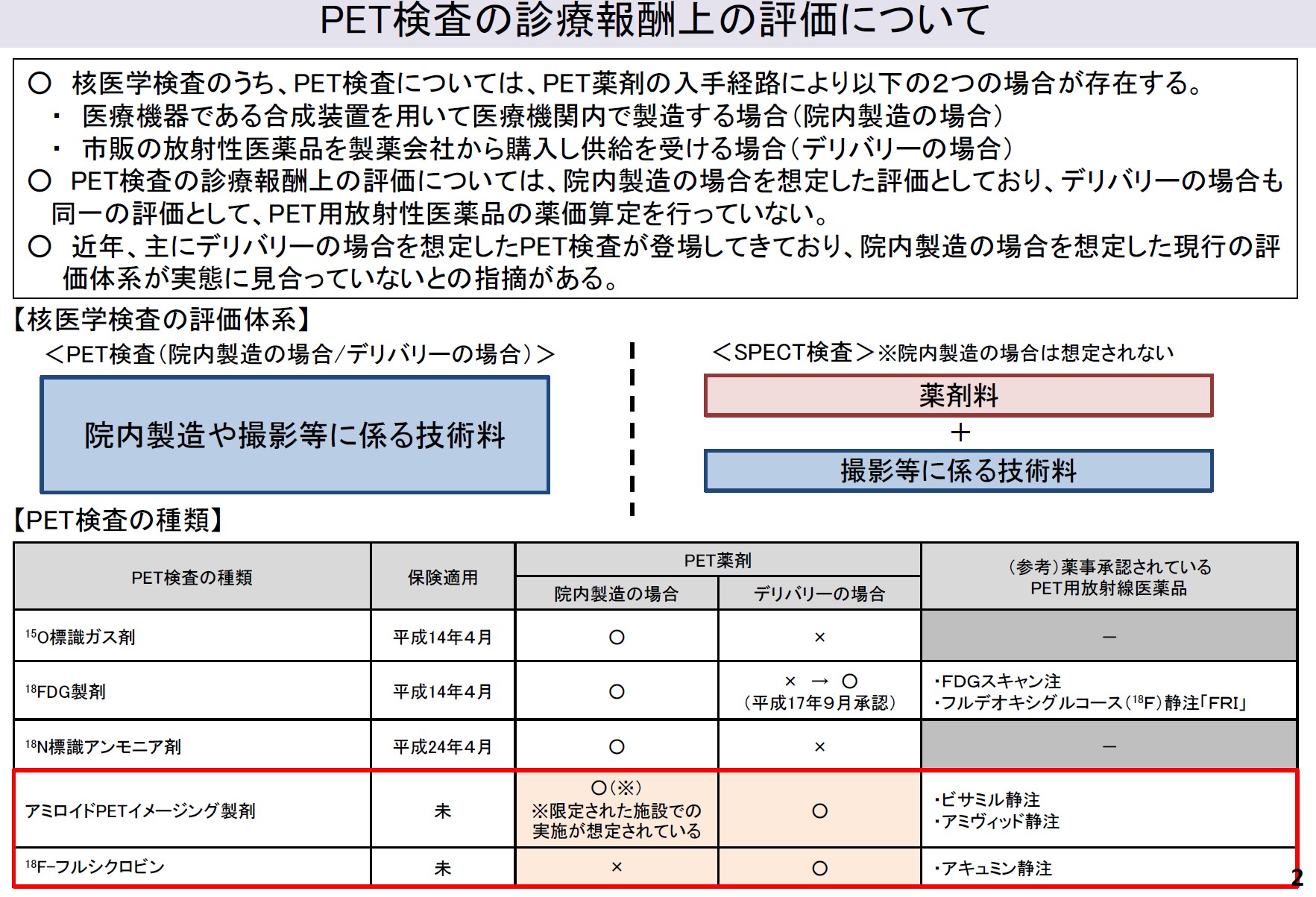
中央社会保険医療協議会 総会(第566回)議事次第|PET検査の診療報酬上の取扱いについて
その他、用法用量変化再算定や費用対効果評価を踏まえた薬価の引き下げも了承され、2024年8月1日より薬価がダウンする薬剤もいくつかありました・・・。

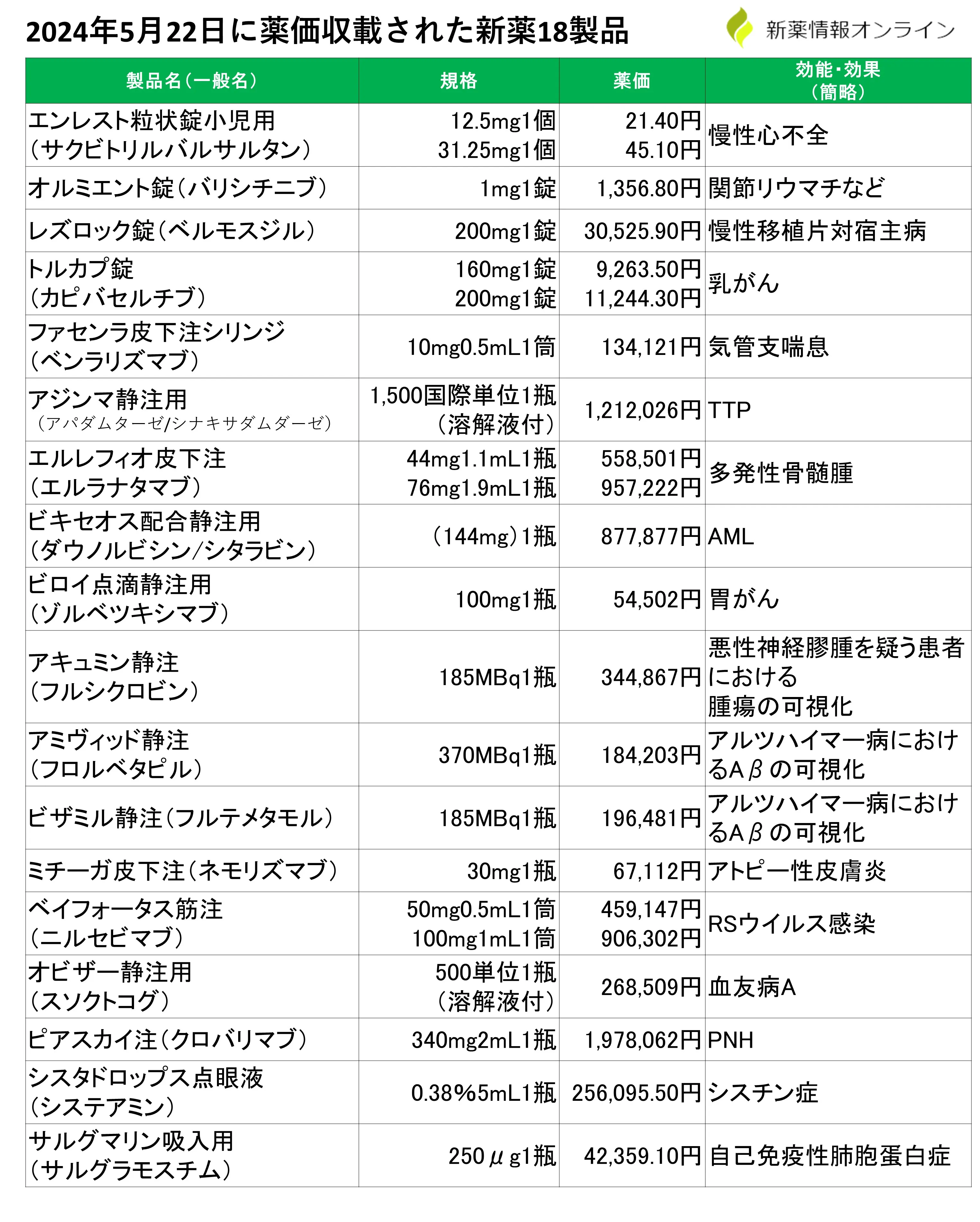
2024年5月22日:薬価収載された18製品
2024年5月22日に薬価収載された新薬一覧は以下の通りです。
| 製品名 (一般名) |
規格 | 薬価 | 効能・効果 (簡略) |
| エンレスト粒状錠小児用 (サクビトリルバルサルタン) |
12.5mg1個 31.25mg1個 |
21.40円 45.10円 |
慢性心不全 |
| オルミエント錠 (バリシチニブ) |
1mg1錠 | 1,356.80円 | 関節リウマチなど |
| レズロック錠 (ベルモスジル) |
200mg1錠 | 30,525.90円 | 慢性移植片対宿主病 |
| トルカプ錠 (カピバセルチブ) |
160mg1錠 200mg1錠 |
9,263.50円 11,244.30円 |
乳がん |
| ファセンラ皮下注シリンジ (ベンラリズマブ) |
10mg0.5mL1筒 | 134,121円 | 気管支喘息 |
| アジンマ静注用 (アパダムターゼ/シナキサダムダーゼ) |
1,500国際単位1瓶 (溶解液付) |
1,212,026円 | TTP |
| エルレフィオ皮下注 (エルラナタマブ) |
44mg1.1mL1瓶 76mg1.9mL1瓶 |
558,501円 957,222円 |
多発性骨髄腫 |
| ビキセオス配合静注用 (ダウノルビシン/シタラビン) |
(144mg)1瓶 | 877,877円 | AML |
| ビロイ点滴静注用 (ゾルベツキシマブ) |
100mg1瓶 | 54,502円 | 胃がん |
| アキュミン静注 (フルシクロビン) |
185MBq1瓶 | 344,867円 | 悪性神経膠腫を疑う患者における 腫瘍の可視化 |
| アミヴィッド静注 (フロルベタピル) |
370MBq1瓶 | 184,203円 | アルツハイマー病におけるAβの可視化 |
| ビザミル静注 (フルテメタモル) |
185MBq1瓶 | 196,481円 | アルツハイマー病におけるAβの可視化 |
| ミチーガ皮下注 (ネモリズマブ) |
30mg1瓶 | 67,112円 | アトピー性皮膚炎 |
| ベイフォータス筋注 (ニルセビマブ) |
50mg0.5mL1筒 100mg1mL1筒 |
459,147円 906,302円 |
RSウイルス感染 |
| オビザー静注用 (スソクトコグ) |
500単位1瓶 (溶解液付) |
268,509円 | 血友病A |
| ピアスカイ注 (クロバリマブ) |
340mg2mL1瓶 | 1,978,062円 | PNH |
| シスタドロップス点眼液 (システアミン) |
0.38%5mL1瓶 | 256,095.50円 | シスチン症 |
| サルグマリン吸入用 (サルグラモスチム) |
250μg1瓶 | 42,359.10円 | 自己免疫性肺胞蛋白症 |
画像はこちらです。>>高画質で表示
薬価の算定方法
各薬剤の薬価算定方法は2024年5月15日の中医協総会の資料に記載されているため、抜粋してご紹介します。
エンレスト粒状錠小児用:規格間調整【加算あり】
エンレスト粒状錠小児用は、エンレスト錠の規格間調整によって算定されました。
また、小児加算(A=20%)の対象でしたので、元の薬価を1.2倍し、以下の薬価に決定しています。
- エンレスト粒状錠小児用12.5mg:21.40円
- エンレスト粒状錠小児用31.25mg:45.10円
なお、加算の根拠は以下の通りです。小児でしっかりと開発を行った点が評価されていますね。
加算の根拠
- 小児加算:本剤は小児に係る用法・用量が明示されていること等から、加算の要件に該当する。日本人の試験組み入れ数等を踏まえ、加算率は20%が妥当である。
ピーク時の予測販売金額は3,800万円です。
作用機序については、以下で解説しています。
-

-
エンレスト(サクビトリルバルサルタン)の作用機序【心不全】
続きを見る

オルミエント錠1mg:規格間調整【加算あり】
オルミエントは、既に4mgと2mg製剤が承認されていましたので、1mg錠はその規格間調整によって算定されました。
また、小児加算(A=15%)の対象でしたので、元の薬価を1.15倍し、以下の薬価に決定しています。
- オルミエント錠1mg:1,356.80円
なお、加算の根拠は以下の通りです。
加算の根拠
- 小児加算:本剤は小児に係る用法・用量が明示されていること等から、加算の要件に該当する。本邦における承認は欧州と比べて大きく遅れていないこと等を踏まえ、加算率は15%が妥当である。
ピーク時の予測販売金額は1.2億円です。
作用機序については、以下で解説しています。
-

-
オルミエント(バリシチニブ)の作用機序【リウマチ/アトピー/COVID-19/円形脱毛症】
続きを見る
現在、JAK阻害薬は多数の薬剤が承認されていますので、以下の記事でまとめています。併せてご参照くださいませ♪
-

-
JAK阻害薬の一覧表(経口7製品)と作用機序のまとめ
続きを見る
レズロック:類似薬効比較方式(Ⅰ)(イムブルビカ)【加算あり】
レズロックは、同じく造血幹細胞移植後の慢性移植片対宿主病に対して使用するイムブルビカ(イブルチニブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。

また、有用性加算(Ⅱ)(A=5%)、市場性加算(Ⅰ)(A=10%)の対象のため、加算前の薬価は26,544.30円でしたが、1.15倍した30,525.90円に決定しました。
- イムブルビカカプセル140mg:8,848.10円(1日薬価:26,544.30円)
- レズロック錠200mg:30,525.90円(1日薬価:30,525.90円)
ピーク時の予測販売金額は22億円です。
トルカプ:類似薬効比較方式(Ⅰ)(イブランス)【加算あり】
トルカプは、同じく乳がんに使用するイブランス(パルボシクリブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、有用性加算(Ⅰ)(A=35%)の対象です。
元々の薬価は200mg1錠 8,329.10円でしたが、1.35倍で11,244.30円です。
- イブランス錠25mg:5,076.80円(1日薬価:19,038.00円)
- トルカプ錠160mg:9,263.50円
- トルカプ錠200mg:11,244.30円(1日薬価:25,701.30円)
なお、加算の根拠は以下の通りです。フルベストラントに対する優越性がしっかりと確認された点が評価されていますね。
加算の根拠
- 有用性加算:本剤はAKT阻害作用を有する新規作用機序医薬品であり、臨床試験において、フルベストラント単独群に対して、フルベストラントに本剤を上乗せした群で有効性が示されたこと等から、有用性加算(Ⅰ)(A=35%)を適用することが適当と判断した。
ピーク時の予測販売金額は103億円です。
作用機序・エビデンスについては以下の記事で解説しています。
-

-
トルカプ(カピバセルチブ)の作用機序【乳がん】
続きを見る
PARP阻害薬のイブランス(パルボシクリブ)とベージニオ(アベマシクリブ)については、以下の記事で解説しています。
-

-
ベージニオ(アベマシクリブ)の作用機序:イブランスとの違い/比較【乳がん】
続きを見る
ファセンラ皮下注10mg:規格間調整【加算あり】
ファセンラは、既に成人用の30mg製剤が承認されています。
そのため、類薬で既に成人・小児製剤のあるヌーカラ皮下注(100mg製剤、小児用40mg製剤)を参考に、規格間調整で算定されました。
また、小児加算(A=15%)の対象です。加算前の薬価は10mg1瓶116,455円でしたが、1.15倍で133,923円となりました。さらにキット特徴部位の原材料費が考慮され、以下に決定しました。
- ファセンラ皮下注10mgシリンジ:134,121円
なお、加算の根拠は以下の通りです。
加算の根拠
- 小児加算:本剤は小児に係る用法・用量が明示されていること等から、加算の要件に該当する。日本人の試験組み入れ数等を踏まえ、加算率は15%が妥当である。
ピーク時の予測販売金額は4,300万円です。
作用機序については、以下で解説しています。
-

-
ファセンラ(ベンラリズマブ)の作用機序と副作用【気管支喘息】
続きを見る
近年では、気管支喘息に使用する生物学的製剤が相次いで登場しています。以下の記事でまとめていますので、併せてご参照くださいませ♪
-

-
テゼスパイア(テゼペルマブ)の作用機序【気管支喘息】
続きを見る

アジンマ:類似薬効比較方式(Ⅰ) (カブリビ)【加算あり】
アジンマは先天性血栓性血小板減少性紫斑病に使用しますが、後天性血栓性血小板減少性紫斑病に使用するカブリビ(カプラシズマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、有用性加算(Ⅰ)(A=40%)、小児加算(A=15%)、迅速導入加算(A=5%)の対象です!!

なお、「迅速導入加算」は2024年度診療報酬改定から導入された新たな加算で、革新的新薬を、海外の承認から遅れることなく日本に導入したことを評価するためのものです。
国内では前回の薬価収載時にボイデヤ錠(ダニコパン)が対象となっていましたので、今回のアジンマが2製品目の対象です。
加算前の薬価は1,500国際単位1瓶 757,516円でしたが、1.6倍の1,212,026円に決定しました。
- カブリビ注射用10mg:515,532円(1日薬価:530,261円)
- アジンマ静注用1500国際単位1瓶:1,212,026円(1日薬価:848,418円)
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:本剤は対象疾患の治療におけるはじめての遺伝子組換えvWF切断酵素(ADAMTS13)であり、「血栓性血小板減少性紫斑病診療ガイド2023」において対象疾患における治療の第一選択として、ADAMTS13の補充を目的とした新鮮凍結人血漿製剤の輸注が推奨されていること、新鮮凍結人血漿製剤の投与と比べて、より少量、かつ、短い時間での投与となって患者負担の軽減につながることから、有用性加算(Ⅰ)(A=40%)を適用することが適当と判断した。
- 小児加算:本剤は小児に係る用法・用量が明示されていること等から、加算の要件に該当する。小児日本人の試験組み入れ数等を踏まえ、加算率は15%が妥当である。
- 迅速導入加算:本剤は国際共同治験により開発され、優先審査の対象であり、かつ本邦における承認申請及び承認は欧米において最も早い承認申請及び承認から6か月以内であることから、加算の要件を満たす。
ピーク時の予測販売金額は33億円です。
作用機序については、以下で解説しています。
-

-
アジンマ(アパダムターゼ/シナキサダムダーゼ)の作用機序【TTP】
続きを見る
エルレフィオ:類似薬効比較方式(Ⅰ)(エプキンリ)【加算あり】
エルレフィオは、造血器腫瘍に使用する二重特異性抗体のエプキンリ(エプコリタマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
エレルフィオは多発性骨髄腫、エプキンリは大細胞型B細胞リンパ腫に使用します。共に二重特異性抗体ですが、標的分子は異なっていますね。
また、有用性加算(Ⅱ)(A=10%)、市場性加算(Ⅰ)(A=10%)の対象です。
元々の薬価は、76mg1瓶 797,685円でしたが、1.2倍されて957,222円に決定しました。
- エプキンリ皮下注48mg:1,595,363円(1日薬価:113,955円)
- エルレフィオ皮下注44mg:558,501円
- エルレフィオ皮下注76mg:957,222円(1日薬価:136,746円)
なお、加算の根拠は以下の通りです。臨床試験で有用性が認められて、標準治療に位置付けられている点が評価されていますね。
加算の根拠
- 有用性加算:臨床試験において再発又は難治性多発性骨髄腫患者における有効性が検証された等、治療方法の改善に該当すること、また、海外の診療ガイドラインにおいて標準的治療法として推奨されていることから、有用性加算(Ⅱ)(A=10%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。
ピーク時の予測販売金額は165億円です。
作用機序とエビデンスについては、以下の記事で解説しています。
-
-
エルレフィオ(エルラナタマブ)の作用機序【多発性骨髄腫】
続きを見る
ビキセオス配合静注用:原価計算方式【加算あり】
ビキセオスは、ダウノルビシンとシタラビンの配合剤ですが、両剤は薬価収載から50年超が経過しており、新薬算定最類似薬は過去10年間に薬価収載されたものとする原則から外れることなどを勘案し、新薬算定最類似薬は存在しないと判断されました。
よって、算定方式は原価計算方式です。
有用性加算(Ⅰ)(A=45%)、市場性加算(Ⅰ)(A=10%)の対象でしたが、原価の開示度が50%未満だったため、加算係数ゼロです。

結果、特に加算は行われずに以下の薬価に決定しました。
- ビキセオス配合静注用:877,877円
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:本剤と強力化学療法(ダウノルビシン・シタラビン併用療法)とを直接比較した臨床試験において、主要評価項目とされたOSについて、対照群に対する本剤群の優越性が検証されたこと、また、既存治療に比して治療日数の短縮等が期待できること等から、有用性加算(Ⅰ)(A=45%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。ただし、本邦における承認が欧米の承認から一定の期間が経過していることを踏まえ、限定的な評価とし、10%とすることが適当と判断した。
ピーク時の予測販売金額は20億円です。
作用機序と特徴は以下の記事で解説しています。
-

-
ビキセオス配合静注用(ダウノルビシン/シタラビン)の作用機序【AML】
続きを見る
ビロイ:類似薬効比較方式(Ⅰ)(オプジーボ)【加算あり】
ビロイは、同じく胃がんに使用するオプジーボ(ニボルマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。

また、有用性加算(Ⅱ)(A=5%)が加算されています。
元々の薬価は、100mg1瓶 51,907円でしたが、1.05倍の上、54,502円に決定しました。
- オプジーボ点滴静注240mg:311,444円(1日薬価:22,246円)
- ビロイ点滴静注用100mg:54,502円(1日薬価:23,358円)
なお、加算の根拠は以下の通りです。新規作用機序である点が評価されていますね。
加算の根拠
- 有用性加算:本剤は、CLDN18.2に選択的に結合し、ADCC活性及びCDC活性を惹起する新規作用機序医薬品であると考えられることから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
ピーク時の予測販売金額は145億円です。
作用機序とエビデンスについては以下で解説しています。
-
-
ビロイ点滴静注用(ゾルベツキシマブ)の作用機序【胃がん】
続きを見る
アキュミン:原価計算方式【加算あり】
アキュミンは、悪性神経膠腫が疑われる患者における腫瘍の可視化に使用する薬剤ですが、同疾患に対する類薬はありません。
そのため、算定方式は原価計算方式です。
有用性加算(Ⅱ)(A=5%)の対象で、原価の開示度が高かった、加算係数は1でした!!ついに、加算係数1!!その結果、以下の薬価に決定しました。
- アキュミン静注185MBq1瓶:344,867円
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:悪性神経膠腫の腫瘍の摘出範囲の決定において、本剤を用いることで摘出範囲の情報を上乗せできる点が評価されているから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
ピーク時の予測販売金額は5.3億円です。
アミヴィッド:原価計算方式【加算あり】
アミヴィッドは、アルツハイマー病による軽度認知障害又は認知症が疑われる患者の脳内アミロイドベータプラークの可視化を目的とする医薬品です。
類薬には、次項のビザミルやフルデオキシグルコース、フルシクロビンがありますが、いずれも薬価未収載のため、類似薬はないと判断されました。
そのため、算定方式は原価計算方式です。
アミヴィッドとビザミルは、共に2023年に承認されたレケンビ(レカネマブ)の投与可否を判断するために使用されます。
検査によってアミロイドβ病理を示唆する所見があって初めてレケンビの投与が可能となります。
-

-
レケンビ(レカネマブ)の作用機序【アルツハイマー型認知症】
続きを見る
また、有用性加算(Ⅱ)(A=10%)の対象で、原価の開示度が高かった、加算係数は1でした。よって、以下の薬価に決定しています。
- アミヴィッド静注370MBq1瓶:184,203円
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:ヒト脳内のアミロイドベータプラークを可視化する既収載品はなく、また、アルツハイマー型認知症の診断においては、バイオマーカーとして脳内のアミロイドベータの蓄積が重視されていること、出荷先に応じて本剤の製造時点での封入量を調節するプロセスは既収載の放射性医薬品にはないことから、有用性加算(Ⅱ)(A=10%)を適用することが適当と判断した。
ピーク時の予測販売金額は11億円です。
ビザミル:原価計算方式【加算あり】
ビザミルも、アミヴィッドと同様の目的(レケンビの投与可否判断)で使用する医薬品です。同様の理由で類似薬はないと判断されました。
そのため、算定方式は原価計算方式です。
また、有用性加算(Ⅱ)(A=5%)の対象で、原価の開示度が高かった、加算係数は1でした。よって、以下の薬価に決定しています。
- ビザミル静注185MBq1瓶:196,481円
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:ヒト脳内のアミロイドベータプラークを可視化する既収載品はなく、また、アルツハイマー型認知症の診断においては、バイオマーカーとして脳内のアミロイドベータの蓄積が重視されていることから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
ピーク時の予測販売金額は41億円です。
-

-
ビザミル(フルテメタモル)の作用機序【アルツハイマー検査薬】
続きを見る
ミチーガ皮下注用30mg:規格間調整【加算あり】
ミチーガは、既に成人用の60mg製剤が承認されていましたので、30mg製剤はその規格間調整によって算定されました。デュピクセントの規格間比を参考に算定されています。
また、小児加算(A=5%)の対象でしたので、元の薬価を1.05倍し、以下の薬価に決定しています。
- ミチーガ皮下注用30mgバイアル:67,112円
なお、加算の根拠は以下の通りです。
加算の根拠
- 小児加算:本剤は小児に係る用法・用量が明示されていること等から、加算の要件に該当する。「既存治療で効果不十分なアトピー性皮膚炎」の効能を有する既収載品が存在していること等を考慮すると、加算率は5%が妥当である。
ピーク時の予測販売金額は44億円です。
作用機序については、以下で解説しています。
-

-
ミチーガ皮下注(ネモリズマブ)の作用機序【アトピー性皮膚炎】
続きを見る
ベイフォータス:類似薬効比較方式(Ⅰ)(シナジス)【加算あり】
ベイフォータスは、同じくRSウイルス感染予防に使用するシナジス(パリビズマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、有用性加算(Ⅱ)(A=5%)、小児加算(A=10%)の対象です。そのため、加算前の薬価は50mg1mL1瓶 399,258円でしたが、1.15倍した459,147円に決定しました。
- シナジス筋注液100mg:102,099円(1シーズン薬価:399,258円)
- ベイフォータス筋注50mgシリンジ:459,147円
- ベイフォータス筋注100mgシリンジ:906,302円(1シーズン薬価:459,147円)
なお、ベイフォータスは、「①重症リスクを有する」場合と「②有さない(健常人)」場合に適応を有していますが、「②有さない(健常人)」に対しては保険対象外とのことです。

また、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:本剤は、類薬であるパリビズマブ(遺伝子組換え)と比較して、投与頻度を低減できること等ことから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
- 小児加算:本剤は小児に係る用法・用量が明示されていること等から、加算の要件に該当する。日本人の試験組み入れ数等を踏まえ、加算率は10%が妥当である。
ピーク時の予測販売金額は179億円です。
作用機序やシナジスの違い等については以下の記事で解説しています。
-

-
ベイフォータス(ニルセビマブ)の作用機序・特徴【RSウイルス感染】
続きを見る
オビザー:原価計算方式【加算あり】
オザビーは、後天性血友病Aに対する補充療法薬です。現在、後天性血友病Aに対しては主にバイパス製剤が使用されていますが、オビザーは直接第Ⅷ因子を補充可能です。
よって、同様の薬理作用及び臨床的位置付けを有する既収載品はないことから新薬算定最類似薬はないと判断されました。
算定方式は原価計算方式です。
また、有用性加算(Ⅱ)(A=10%)、市場性加算(I)(A=10%)の対象で、加算係数は0.6でした。
よって、元々の薬価は349,815円でしたが、1.12倍(20%×0.6)の268,509円に決定しました。
- オビザー静注用500単位1瓶(溶解液付):268,509円
なお、加算の根拠は以下の通りです。ピーク時の投与患者数予想は「5人」ですので、かなりの希少疾病です。
加算の根拠
- 有用性加算:本剤は、ブタ血液凝固第Ⅷ因子の構造を一部改変したことで、自己抗体の影響を受けず、直接的にFⅧとして作用を発揮することから有用性加算(Ⅱ)(A=10%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。ただし、本邦における承認が欧米の承認から一定の期間が経過していることを踏まえ、限定的な評価とし、10%とすること適当と判断した。
ピーク時の予測販売金額は7,400万円です。
参考までに、後天性血友病Aに対しては、二重特異性抗体のヘムライブラ(エミシズマブ)が使用可能です。
-

-
ヘムライブラ(エミシズマブ)の作用機序と二重特異性抗体【血友病A】
続きを見る
ピアスカイ注:類似薬効比較方式(Ⅰ) (ユルトミリス)【加算あり】
ピアスカイは、同じく発作性夜間ヘモグロビン尿症に使用する抗補体C5抗体薬のユルトミリス(ラブリズマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、有用性加算(Ⅱ)(A=5%)、小児加算(A=10%)の対象です。加算前の薬価は1,720,054円でしたが、1.15倍されて1,978,062円に決定しました。
- ユルトミリスHI点滴静注300mg:659,985円(1日薬価:122,861円)
- ピアスカイ注340mg:1,978,062円(1日薬価:141,290円)
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:本剤は、補体阻害剤の治療歴のある患者を対象とした国際共同第Ⅲ相試験も実施し、有効性が確認されていることから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
- 小児加算:本剤は小児に係る用法・用量が明示された初めてのC5阻害剤であること等から、加算の要件に該当する。18歳未満の日本人症例の組み入れがなかったこと等から、加算率は10%が妥当である。
ピーク時の予測販売金額は105億円です。
作用機序や既存の抗補体C5抗体薬との違いについては、以下で解説しています。
-

-
ピアスカイ(クロバリマブ)の作用機序【PNH】
続きを見る
シスタドロップス:原価計算方式【加算あり】
シスタドロップス点眼液は、「シスチン症における角膜シスチン結晶の減少」を効能・効果とする医薬品です。
腎性シスチン症治療に使用する類薬のニシスタゴン(システアミン酒石酸塩)は、一定程度の類似性があると考えられるものの、効能・効果や投与形態・剤形が異なることから、類似薬はないと判断されました。
よって、算定方式は原価計算方式です。
また、有用性加算(Ⅱ)(A=15%)、市場性加算(I)(A=10%)の対象で、加算係数は0.6でした。また、外国平均価格調整が行われ、以下の薬価に決定しました。
- シスタドロップス点眼液0.38%5mL1瓶:256,095.50円
なお、加算の根拠は以下の通りです。臨床試験で有用性が認められて、標準治療に位置付けられている点が評価されていますね。
加算の根拠
- 有用性加算:本剤は既存 の治療 方法が なかった対 象疾病 に対し 、症状の改 善に寄 与する こと、標準治療法として位置づけられると考えられること、副次評価項目である羞明スコアにおいて改善傾向が示されていることから、有用性加算(Ⅱ)(A=15%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。
ピーク時の予測販売金額は3.5億円です。
サルグマリン:原価計算方式【加算あり】
サルグマリンと同様の効能・効果、薬理作用及び臨床的位置づけを有する既収載品はないことから新薬算定最類似薬はないと判断されました。
よって、算定方式は原価計算方式です。
画期性加算(A=75%)、市場性加算(Ⅰ)(A=15%)の対象でしたが、原価の開示度が50%未満だったため、加算係数ゼロです。

結果、特に加算は行われずに以下の薬価に決定しました。
- サルグマリン吸入用250μg:42,359.10円
なお、加算の根拠は以下の通りです。
加算の根拠
- 画期性加算:本剤は既存のコロニー刺激因子製剤と異なり肺胞で作用を発現すること、標準治療と異なり現時点では安全性上の重大な懸念は示されていないこと等から、画期性加算(A=75%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。
ピーク時の予測販売金額は4.2億円です。
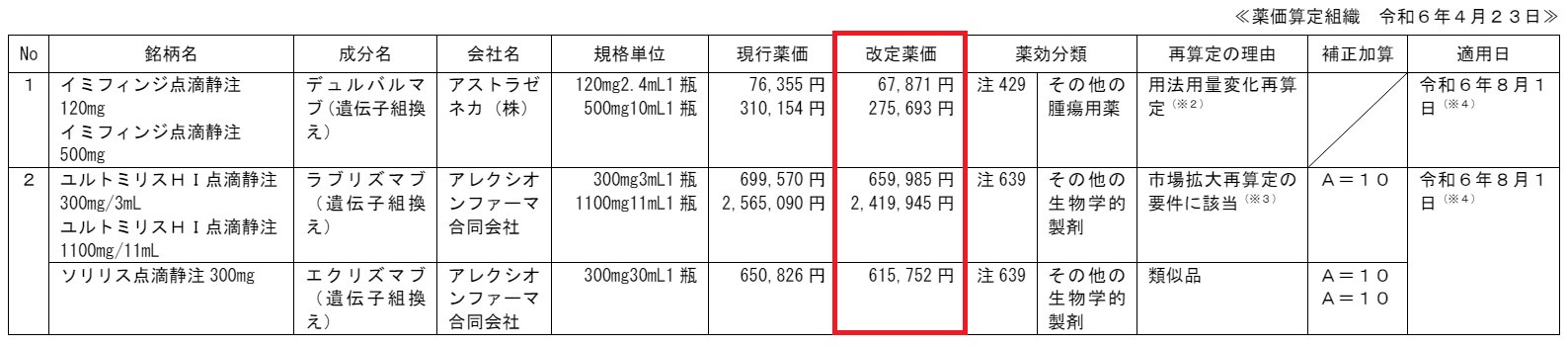
用法用量変化再算定&市場拡大再算定:イミフィンジ、ユルトミリス、ソリリス
効能変更等が承認された既収載品及び2年度目以降の予想販売額が一定規模を超える市場拡大のあった場合、新薬収載の機会(年4回)を活用して、薬価を見直すこととされています。
イミフィンジ(デュルバルマブ)は、2022年12月23日に「治癒切除不能な胆道がん」、「切除不能な進行・再発の非小細胞肺がん」、「切除不能な肝細胞がん」の適応拡大が承認され、市場規模が増加したことから、2024年2月1日に薬価が引き下げられたばかりです(参考:市場拡大再算定の決定)。
その後、2023年11月24日に用法用量の変更(変更前:1回10mg/kgを2週間間隔投与→変更後:1回1500mgを4週間隔投与)が行われましたので、用法用量変化再算定の要件に該当し、薬価が引き下げられます。
-

-
イミフィンジ(デュルバルマブ)の作用機序と副作用【肺/胆/肝/子宮体がん】
続きを見る
また、ユルトミリス(ラブリズマブ)は2023年5年25日に「視神経脊髄炎スペクトラム障害(視神経脊髄炎を含む)の再発予防」の適応拡大が承認されたため、市場拡大再算定によって薬価が引き下げられます。
その類似品のソリリス点滴静注は、道連れでの薬価引き下げです。
-

-
ユルトミリス(ラブリズマブ)の作用機序:ソリリスとの違い【PNH】
続きを見る
その結果、2024年8月1日より、現在販売されている上記医薬品の薬価は以下に引き下げられます。
イミフィンジは11.1%、ユルトミリスは5.7%、ソリリスは5.4%の薬価ダウンです。
費用対効果評価:ソーティクツ
中医協総会では、費用対効果評価も行われ、ソーティクツ(デュークラバシチニブ)についても2024年8月1日より薬価が下がります。
- ソーティクツ(デュークラバシチニブ) 6mg1 錠:2,770.90 円 → 2,533.40 円

あとがき
今回は18製品中、全ての新薬が加算対象でした!珍しいですね!!

以上、今回は2024年5月22日に薬価収載された新薬18製品についてご紹介しました!
\ 新薬情報オンラインの運営者が執筆! /
薬剤師におススメの記事
失敗しない薬剤師の転職とは?
数多く存在する薬剤師専門の転職エージェントサイト。
どこに登録したらいいのか悩むことも少なくありません。そんな転職をご検討の薬剤師さんに是非見ていただきたい記事を公開しました。
- 新薬情報オンラインの薬剤師2名が実際に利用・取材!
- 各サイトの特徴等を一覧表で分かりやすく掲載!
- 絶対にハズレのない厳選の3サイトを解説!
上手に活用してあなたの希望・条件に沿った【失敗しない転職】を実現していただけると嬉しいです!
-

-
薬剤師の転職サイト3選|評判・求人特徴とエージェントの質を比較
続きを見る

日々の情報収集に最適
-

-
薬剤師の勉強・情報収集に役に立つ無料サイト・ブログ8選


































