PASSMED公式LINEの登録者特典|当サイトに掲載している図表の元データ&学習支援AI 薬科GPTをプレゼント♪
2024年11月20日、新薬17製品が薬価収載されました!
前回から見送られていた週1回投与の基礎インスリン製剤アウィクリ注(インスリン イコデク)が今回登場です。
-

-
アウィクリ注(インスリン イコデク)の作用機序・特徴【糖尿病】
続きを見る
今回はアウィクリも注目ですが、新規作用機序のフリュザクラ(フルキンチニブ)やトロデルビ(サシツズマブ ゴビテカン)やライブリバント(アミバンタマブ)、レケンビ(レカネマブ)に次ぐ2製品目の抗アミロイドβ抗体薬ケサンラ(ドナネマブ)なども注目です。
その他、費用対効果評価を踏まえた薬価の引き下げも了承され、2025年2月1日より薬価がダウンする薬剤もいくつかありました・・・。

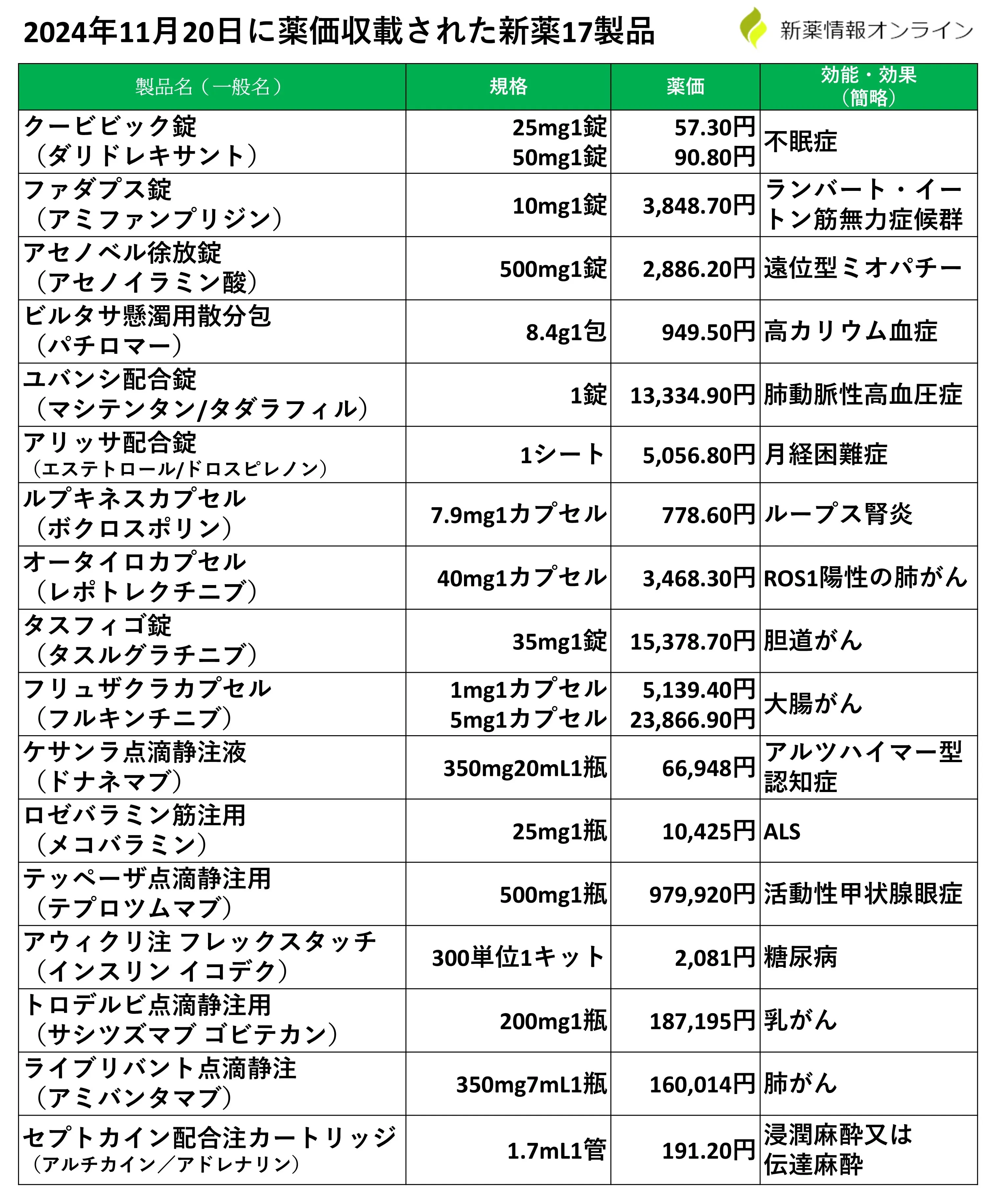
2024年11月20日:薬価収載された17製品
2024年11月20日に薬価収載された新薬一覧は以下の通りです。
| 製品名 (一般名) |
規格 | 薬価 | 効能・効果 (簡略) |
| クービビック錠 (ダリドレキサント) |
25mg1錠 50mg1錠 |
57.30円 90.80円 |
不眠症 |
| ファダプス錠 (アミファンプリジン) |
10mg1錠 | 3,848.70円 | ランバート・イートン筋無力症候群 |
| アセノベル徐放錠 (アセノイラミン酸) |
500mg1錠 | 2,886.20円 | 遠位型ミオパチー |
| ビルタサ懸濁用散分包 (パチロマー) |
8.4g1包 | 949.50円 | 高カリウム血症 |
| ユバンシ配合錠 (マシテンタン/タダラフィル) |
1錠 | 13,334.90円 | 肺動脈性高血圧症 |
| アリッサ配合錠 (エステトロール/ドロスピレノン) |
1シート | 5,056.80円 | 月経困難症 |
| ルプキネスカプセル (ボクロスポリン) |
7.9mg1カプセル | 778.60円 | ループス腎炎 |
| オータイロカプセル (レポトレクチニブ) |
40mg1カプセル | 3,468.30円 | ROS1陽性の肺がん |
| タスフィゴ錠 (タスルグラチニブ) |
35mg1錠 | 15,378.70円 | 胆道がん |
| フリュザクラカプセル (フルキンチニブ) |
1mg1カプセル 5mg1カプセル |
5,139.40円 23,866.90円 |
大腸がん |
| ケサンラ点滴静注液 (ドナネマブ) |
350mg20mL1瓶 | 66,948円 | アルツハイマー型認知症 |
| ロゼバラミン筋注用 (メコバラミン) |
25mg1瓶 | 10,425円 | ALS |
| テッペーザ点滴静注用 (テプロツムマブ) |
500mg1瓶 | 979,920円 | 活動性甲状腺眼症 |
| アウィクリ注 フレックスタッチ (インスリン イコデク) |
300単位1キット | 2,081円 | 糖尿病 |
| トロデルビ点滴静注用 (サシツズマブ ゴビテカン) |
200mg1瓶 | 187,195円 | 乳がん |
| ライブリバント点滴静注 (アミバンタマブ) |
350mg7mL1瓶 | 160,014円 | 肺がん |
| セプトカイン配合注カートリッジ (アルチカイン/アドレナリン) |
1.7mL1管 | 191.20円 | 浸潤麻酔又は伝達麻酔 |
画像はこちらです。>>高画質で表示
薬価の算定方法
各薬剤の薬価算定方法は2024年11月13日の中医協総会の資料に記載されているため、抜粋してご紹介します。
クービビック錠:類似薬効比較方式(Ⅰ)(ベルソムラ)
クービビックは同じく不眠症に使用する同作用機序のベルソムラ(スボレキサント)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
不服意見はあったものの、特に加算はなく以下の薬価に決定しています。
- ベルソムラ錠15mg:90.80円(1日薬価:90.80円)
- クービビック錠25mg:57.30円
- クービビック錠50mg:90.80円(1日薬価:90.80円)
ちなみに、1日薬価算定時に汎用規格を「25mg」とすべきとの不服意見がありましたが、用法・用量は「50mg」が基本となっているため、残念ながら却下されました。
- 汎用規格は、添付文書の用法・用量の記載ではなく、実際の使用量に基づいて決定されるべきである。
- 他剤の使用実績は、低用量での使用が最も多くなっている。本剤でも低用量での使用が最も多くなると予想されるため低用量の25mgが汎用規格と考える。
↓↓↓
- 本剤の承認された用法及び用量や、審査報告書において「臨床試験において本剤50mg投与により有効性が検証され、かつ25mg投与より高い効果が期待できること、安全性の観点では、本剤50mg投与を避けるべきと考えられるような事象は認められておらず、本剤25mg投与時と比較してリスクが明らかに高くなる傾向もないことから、本剤の通常用量は50mgとし、患者の状態に応じて、医師の判断により25mgに減量可能とすることが適切であると考える。」と評価されていることを踏まえると、汎用規格は50mgとすることが妥当と判断する。

ピーク時の予測販売金額は199億円です(予測本剤投与患者数118万人)。
作用機序や類薬(デエビゴ、ベルソムラ)との違いについては、以下で解説しています。
-

-
クービビック(ダリドレキサント)の作用機序【不眠症】
続きを見る
ファダプス錠:原価計算方式【加算あり】
ファダプスと同様の効能・効果、薬理作用を有する既収載品はないことから新薬算定最類似薬はないと判断されました。
よって、算定方式は原価計算方式です。
有用性加算(Ⅱ)(A=5%)、市場性加算(Ⅰ)(A=10%)の対象でしたが、原価の開示度が50%未満だったため、加算係数ゼロです。

結果、特に加算は行われずに以下の薬価に決定しました。
- ファダプス錠10mg:3,848.70円
なお、加算の根拠は以下の通りです。国内外のガイドラインで第一選択薬として推奨されている点が評価されましたね。
加算の根拠
- 有用性加算:本剤は国内外の診療ガイドラインで治療の第一選択として推奨されていることから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす
ピーク時の予測販売金額は10億円です(予測本剤投与患者数205人)。
アセノベル徐放錠:原価計算方式【加算あり】
アセノベルと同様の効能・効果、薬理作用を有する既収載品はないことから新薬算定最類似薬はないと判断されました。
よって、算定方式は原価計算方式です。
また、有用性加算(Ⅰ)(A=45%)、市場性加算(Ⅰ)(A=10%)、迅速導入加算(A=5%)の対象です!!アセノベルは原価の開示度が80%以上と高かったことから加算係数は1.0でした。

ちなみに、「迅速導入加算」は2024年度診療報酬改定から導入された新たな加算で、革新的新薬を、海外の承認から遅れることなく日本に導入したことを評価するためのものです。
結果、当初薬価から1.6倍された以下の薬価に決定しました。
- アセノベル徐放錠500mg:2,886.20円
なお、加算の根拠は以下の通りです。新規作用機序かつ標準治療となり得ることが評価されましたね。
加算の根拠
- 有用性加算:本剤はシアル酸を補充することにより効果を示すことが期待されている新規作用機序の薬剤であること、対象疾患は国内外において治療法が存在しない重篤な疾患であること、また、本剤は補充療法であり他に治療法がないことから標準的治療法となると考えられることから、有用性加算(Ⅰ)(A=45%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。
- 迅速導入加算:本剤は日本以外の国と同時に臨床試験を実施して開発され、優先審査の対象であり、かつ欧米では承認申請及び承認されていない品目であることから、加算の要件を満たす。
有用性加算の対象範囲や、原価の考え方について不服意見がありましたが、一部は却下されていました。
- 対象疾患に確立した治療法はなく、本剤は第一選択薬として標準的治療に位置づけられ、ガイドライン等に記載される予定であることから、有用性加算の要件③-bを満たす。
- 本剤は、GNE遺伝子変異によって発症する本疾患に対してのみ有用であり、臨床試験において、プラセボ群と比較して本剤群で高い効果が示されていることから、有用性加算の要件③-eを満たす。
- 承認申請に必要な試験データの対価である大学へのロイヤリティは、本剤の承認申請に必要な試験データにかかる費用であるため、研究開発費用に計上されることが妥当である。
↓↓↓
- 本剤の対象疾患の患者数は極めて少なく、確立した治療法が国内外問わず存在しないこと、本剤の作用機序は遺伝子変異により欠乏した成分を補充するものであること等を踏まえ、総合的に判断し、有用性加算の要件③-bに該当する。
- 有用性加算の要件③-eは、原則、類似薬効比較方式で算定された医薬品に対する評価項目であるが本剤の算定方式は原価計算方式であり、また、本剤の臨床試験成績から高い効果が示されているとの判断はできず、有用性加算の要件③-eには該当しない。
- 国内第Ⅲ相試験等は主に公的研究費により実施されたものであり、大学へのロイヤリティは研究開発費用としては認めないことが妥当と判断する。
ピーク時の予測販売金額は9.8億円です(予測本剤投与患者数193人)。
ビルタサ懸濁用散分包:類似薬効比較方式(Ⅰ)(ロケルマ)
ビルタサは、同じく高カリウム血症に使用するロケルマ(ジルコニウムシクロケイ酸)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
特に加算はなく、以下の薬価に決定しました。
- ロケルマ懸濁用散分包5g:1,024.30円(1日薬価:1,517.90円)
- ビルタサ懸濁用散分包8.4g1包:949.50円(1日薬価:1,517.90円)
ピーク時の予測販売金額は40億円です(予測本剤投与患者数18.6千人)。
作用機序やロケルマとの違いについては以下の記事で解説しています。
-
-
ビルタサ(パチロマーソルビテクスカルシウム)の作用機序・特徴【高K血症】
続きを見る
ユバンシ配合錠:新医療用配合剤の特例
ユバンシ配合錠は、既に肺動脈性肺高血圧症で使用されている以下の2つの薬剤の合剤です。
- ①オプスミット(マシテンタン):エンドセリン受容体拮抗薬
- ②アドシルカ(タダラフィル):PDE5阻害薬
①についてはヤンセンファーマ社の自社製品のため、新医療用配合剤の特例として「自社品の薬価×0.8+他社品の最低薬価」により算定されました。
しかし、計算した結果、マシテンタン10mg錠単剤の薬価を下回ったため、ユバンシの薬価はオプスミット錠10mgの薬価と同額とされました。
特に加算はなく、以下の薬価に決定しました。
- ユバンシ配合錠 1錠:13,334.90円(1日薬価:13,334.90円)
ピーク時の予測販売金額は107億円です(予測本剤投与患者数2.5千人)。
作用機序については、以下で解説しています。
-

-
ユバンシ配合錠(マシテンタン/タダラフィル)の作用機序【肺動脈性高血圧症】
続きを見る
また、既存薬の配合薬であることから、14日の処方日数の制限は設けないことが了承されています。
アリッサ配合錠:類似薬効比較方式(Ⅱ) (既存類薬平均薬価)
アリッサ配合錠と同様の効能・効果、作用機序を有する類薬は、既にいくつか承認・販売されています。
- ルナベル配合錠(一般名:ノルエチステロン/エチニルエストラジオール)
- ヤーズ配合錠(一般名:ドロスピレノン/エチニルエストラジオール)
- ヤーズフレックス配合錠(一般名:ドロスピレノン/エチニルエストラジオール)
- ジェミーナ配合錠(一般名:レボノルゲストレル/エチニルエストラジオール)
そのため、類似薬効比較方式(Ⅱ)として、過去15年間に薬価収載された薬理作用類似薬の平均1日薬価を元に算出されました。
特に加算はなく、以下の薬価に決定しました。
- アリッサ配合錠 1シート:5,056.80円(1日薬価:180.60円)
ピーク時の予測販売金額は75億円です(予測本剤投与患者数186千人)。
作用機序・特徴については、以下で解説しています。
-

-
アリッサ配合錠(エステトロール/ドロスピレノン)の作用機序【月経困難症】
続きを見る
また、アリッサはシート単位の処方であり、28日間の投与(プレセボ含む)です。そのため、14日の処方日数の制限を「30日」にすることが了承されています。
ルプキネスカプセル:原価計算方式【加算あり】
ルプキネスと類似の効能・効果及び薬理作用を有するタクロリムス水和物は、G1/G2品目であることから、薬価算定上の最類似薬には原則として選定しないとされました。また、その他、本剤と同様の効能・効果及び薬理作用を有する既収載品はないことから、新薬算定最類似薬はないと判断されています。
よって、算定方式は原価計算方式です。
また、有用性加算(Ⅱ)(A=5%)の対象で、原価の開示度が50%以上80%未満だったため、加算係数0.6とされました。
元々の薬価は、7.9mg1カプセル 755.90円でしたが、1.03倍(5%×0.6=3%加算)されて778.60円に決定しました。
- ルプキネスカプセル7.9mg:778.60円
なお、加算の根拠は以下の通りです。臨床試験で有用性が認められたことが評価されていますね。
加算の根拠
- 有用性加算:本剤の臨床試験において、既存の標準的な一次治療に対する本剤の上乗せ効果が示されたことから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
ピーク時の予測販売金額は23億円です(予測本剤投与患者数3.2千人)。
オータイロカプセル:類似薬効比較方式(Ⅰ)(ロズリートレク)
オータイロは、同じくROS1融合遺伝子陽性の切除不能な進行・再発の非小細胞肺がんに使用するROS1阻害薬のロズリートレク(エヌトレクチニブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
特に加算はなく、以下の薬価に決定しました。
- ロズリートレクカプセル200mg:10,073.00円(1日薬価:27,746.40円)
- オータイロカプセル40mg:3,468.30円(1日薬価:27,746.40円)
ピーク時の予測販売金額は21億円です(予測本剤投与患者数253人)。
作用機序は以下の記事で解説しています。
-
-
オータイロ(レポトレクチニブ)の作用機序【ROS1陽性の肺がん】
続きを見る
タスフィゴ錠:類似薬効比較方式(Ⅰ)(リトゴビ)【加算あり】
タスフィゴは、同じく胆道がんに使用する経口FGFR阻害薬のリトゴビ(フチバチニブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、市場性加算(Ⅰ)(A=10%)、迅速導入加算(A=10%)が加算されています。
元々の薬価は、35mg1錠 12,815.60円でしたが、1.2倍の15,378.70円に決定しました。
- リトゴビ錠4mg:10,252.50円(1日薬価:51,262.50円)
- タスフィゴ錠35mg:15,378.70円(1日薬価:61,514.80円)
なお、加算の根拠は以下の通りです。
加算の根拠
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。
- 迅速導入加算:本剤は国際共同治験により開発され、優先審査の対象であり、かつ本邦における承認申請及び承認は欧米より早いことから、加算の要件を満たす。国際共同治験における日本人症例数が比較的多いことを踏まえ、加算率は10%が妥当である。
ピーク時の予測販売金額は3.6億円です(予測本剤投与患者数51人)。
作用機序とエビデンスについては以下で解説しています。
-
-
タスフィゴ(タスルグラチニブ)の作用機序【胆道がん】
続きを見る
フリュザクラ:類似薬効比較方式(Ⅰ)(スチバーガ)【加算あり】
フリュザクラは、同じく大腸がんの後方ラインで使用するマルチキナーゼ阻害薬のスチバーガ(レゴラフェニブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
有用性加算(Ⅱ)(A=5%)の対象のため、1.05倍された以下の薬価に決定しました。
- スチバーガ錠40mg:5,682.60円(1日薬価:17,047.80円)
- フリュザクラカプセル1mg:5,139.40円
- フリュザクラカプセル5mg:23,866.90円(1日薬価:17,900.20円)

加算の根拠
- 有用性加算:本剤は、化学療法歴があり、トリフルリジン・チピラシル塩酸塩又はレゴラフェニブに不応又は不耐の治癒切除不能な進行・再発の結腸・直腸癌患者において、主要評価項目のOSについてプラセボ群に対する本剤群の優越性が検証されていることから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
ピーク時の予測販売金額は25億円です(予測本剤投与患者数1.6千人)。
作用機序とエビデンスについては以下で解説しています。
-
-
フリュザクラ(フルキンチニブ)の作用機序【大腸がん】
続きを見る
ケサンラ点滴静注液:類似薬効比較方式(Ⅰ)(レケンビ)【加算あり】
ケサンラは、同じくアルツハイマー型認知症に使用する抗アミロイドβ抗体薬のレケンビ(レカネマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
有用性加算(Ⅱ)(A=5%)の対象のため、1.05倍された以下の薬価に決定しています。
- レケンビ点滴静注200mg:45,777円(1日薬価:8,152円)
- ケサンラ点滴静注液350mg:66,948円(1日薬価:8,560円)

加算の根拠
- 有用性加算:本剤は、投与を18か月間継続する比較薬と異なり、添付文書において、投与期間が原則18か月間とされた上で、投与開始後12か月を目安に行われる評価で、アミロイドβプラーク除去が確認された場合は投与を完了することとされていることから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
また、1日薬価算出に当たって、体重および投与期間に関する不服意見がありましたが、却下されていました。
- 1日薬価の算出に用いる体重及び投与期間は以下のとおりとすることが適切と考える。
- 比較薬の1日薬価の計算に用いる体重として、比較薬の国際共同第Ⅲ相試験における日本人被験者の平均体重を用いる。
- 本剤は投与開始後12か月を目安に行われる評価で、アミロイドβプラーク除去が確認された場合は投与を完了することとされていることから、本剤の投与期間の計算にあたっては臨床試験の結果(12か月で投与完了する患者割合)を考慮する。
↓↓↓
- 以下の理由から、比較薬の1日薬価の算出に用いる体重は50kg、本剤の投与期間は18か月とすることが妥当と判断する。
- 体重当たりの投与量が設定された薬剤では、通常、成人の場合は50kgを用いて1日薬価を算出しており、臨床試験における平均体重を用いる合理的な理由はない。
- 比較薬より早期に投与完了できる点は有用性加算の③-cで既に評価している。
ピーク時の予測販売金額は796億円です(予測本剤投与患者数2.6万人)。
作用機序とエビデンス、レケンビとの違いについては以下で解説しています。
-

-
ケサンラ(ドナネマブ)の作用機序:レケンビとの違い【アルツハイマー型認知症】
続きを見る
ロゼバラミン筋注用:原価計算方式【加算あり】
ロゼバラミンの有効成分はメコバラミンであり、既に製品名メチコバールとして承認・販売されています。今回登場したロゼバラミンはメコバラミンの高用量製剤ですが、単純な規格差では算出できません。
そのため、「組成及び投与形態が同一で効能及び効果が異なる既収載品がある新薬の薬価算定の特例」として原価計算方式で算定されました。
また、市場性加算(Ⅰ)(A=10%)の対象で、原価の開示度が50%以上80%未満だったため、加算係数0.6とされました。よって、以下の薬価に決定しています。
- ロゼバラミン筋注用25mg:10,425円
なお、加算の根拠は以下の通りです。
加算の根拠
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。
ピーク時の予測販売金額は27億円です(予測本剤投与患者数1.3千人)。
以下の記事で作用機序やエビデンスについて解説しています。
-

-
ロゼバラミン筋注用(メコバラミン)の作用機序【ALS】
続きを見る
テッペーザ点滴静注用:原価計算方式【加算あり】
テッペーザと同様の効能・効果、薬理作用を有する既収載品はないこと等から薬価算定最類似薬はないと判断されました。
よって、原価計算方式で算定されています。
また、有用性加算(Ⅰ)(A=45%)、市場性加算(Ⅰ)(A=10%)の対象でしたが、原価の開示度が50%未満だったため、加算係数ゼロです。
- テッペーザ点滴静注用500mg:979,920円
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:本剤はIGF-1受容体阻害作用を有する新規作用機序医薬品であること、投与対象は主に中等度から重度の活動性甲状腺眼症患者であり、臨床試験成績から当該対象に対して臨床的に意義のある改善が示されていること等から、有用性加算(Ⅰ)(A=45%)を適用することが適当と判断した。
- 市場性加算:本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。
ピーク時の予測販売金額は494億円です(予測本剤投与患者数3.4千人)。
作用機序やエビデンスについては以下で解説しています。
-
-
テッペーザ(テプロツムマブ)の作用機序【甲状腺眼症】
続きを見る
アウィクリ注:類似薬効比較方式(Ⅰ)(トレシーバ)【加算あり】
アウィクリは、同じくインスリン製剤のトレシーバ(インスリン デグルデク)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、有用性加算(Ⅱ)(A=5%)の対象です。そのため、加算前の薬価は300単位1キット 1,296円でしたが、1.05倍の2,081円に決定しました。
- トレシーバ注ペンフィル(300単位1筒):1,438円(1日薬価:519円)
- アウィクリ注 フレックスタッチ300単位1キット:2,081円(1日薬価:555円)

加算の根拠
- 有用性加算:本剤は、週1回投与の持効型インスリンであり、比較薬と比べて注射頻度の減少による患者負担の軽減が期待されることから、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
また、さらなる加算の追加に対する不服意見がありましたが、全て却下されていました。
- 既存薬と比較してHbA1cの目標値7%未満及び低血糖を発現せずにHbA1cの目標値7%未満の達成率並びにTIR(目標血糖値範囲)が有意に高い結果が示されており、良好な血糖コントロールと生命予後に寄与すると考えることから、有用性加算の要件③-fを満たす。
↓↓↓
- TIRの改善について、現時点では生命予後等に寄与する評価項目としての臨床的意義が確立しているとまでは判断できず、審査報告書において「特に1型糖尿病患者に本剤を投与する場合は、低血糖の発現が多かった臨床試験成績を踏まえ、…適切な血糖コントロールが得られない場合は既存の連日投与のBasalインスリン製剤に切り替える旨を注意喚起することが適切」と評価されていることも踏まえると、有用性加算の要件③-fには該当しない。
ピーク時の予測販売金額は131億円です(予測本剤投与患者数308千人)。
作用機序や特徴については以下の記事で解説しています。
-

-
アウィクリ注(インスリン イコデク)の作用機序・特徴【糖尿病】
続きを見る
トロデルビ点滴静注用:類似薬効比較方式(Ⅰ)(テセントリク)【加算あり】
トロデルビは国内初の抗TROP2抗体ですが、薬価算定においては同じく乳がんに使用する免疫チェックポイント阻害薬のテセントリク(アテゾリズマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、有用性加算(Ⅰ)(A=40%) の対象のため、元々の薬価を1.4倍した以下に決定しました。
- テセントリク点滴静注840mg:445,699円(1日薬価:31,836円)
- トロデルビ点滴静注用200mg:187,195円(1日薬価:44,570円)
なお、加算の根拠は以下の通りです。
加算の根拠
- 有用性加算:本剤は、適応患者を踏まえると新たにTROP-2をターゲットとすることに一定の意義があると考えられたこと、未承認薬検討会議で開発要望があり、申請者が米国会社の買収後に本邦での開発に着手し、ドラッグロス品目の着実な開発について一定の評価が可能であること、第Ⅲ相試験において既存の化学療法群と比べて本剤群でOSの有意な延長が示されたことから、有用性加算(Ⅰ)(A=40%)を適用することが適当と判断した。
ピーク時の予測販売金額は93億円です(予測本剤投与患者数1.7千人)。
作用機序や特徴については、以下の記事で解説しています。
-

-
トロデルビ(サシツズマブ ゴビテカン)の作用機序【乳がん】
続きを見る
ライブリバント点滴静注:類似薬効比較方式(Ⅰ) (ポートラーザ)【加算あり】
ライブリバントは国内初のEGFRとMETの二重特異性抗体です。同じく非小細胞肺がんに使用し、EGFRをターゲットとする抗体薬のポートラーザ(ネシツムマブ)の1日薬価に合わせて算定されました。
算定方式は類似薬効比較方式(Ⅰ)です。
また、有用性加算(Ⅱ)(A=10%)の対象です。元の薬価から1.1倍され、さらに外国平均価格調整が行われて以下の薬価に決定しました。
- ポートラーザ点滴静注液800mg:228,328円(1日薬価:21,746円)
- ライブリバント点滴静注350mg:160,014円(1日薬価:38,099円)

加算の根拠
- 有用性加算:本剤は、米国NCCNガイドラインの記載等から標準的治療に位置づけられると考えられること、臨床試験において、カルボプラチンとペメトレキセドの併用群に対して、当該併用に本剤を上乗せした群で有効性が示されたこと等から、有用性加算(Ⅱ)(A=10%)を適用することが適当と判断した。
ピーク時の予測販売金額は22億円です(予測本剤投与患者数416人)。
作用機序や特徴・エビデンスについては、以下で解説しています。
-

-
リブロファズ/ライブリバント(アミバンタマブ)の作用機序【肺がん】
続きを見る
セプトカイン配合注:原価計算方式
セプトカインは麻酔薬のため、メピバカイン塩酸塩、プロピトカイン塩酸塩・フェリプレシン及びリドカイン塩酸塩・アドレナリンは一定の類似性があると
考えられるものの、これらの薬剤はいずれも薬価収載から20年超が経過した品目であり、新薬算定上の最類似薬には原則として該当せず、新薬算定最類似薬はないと判断されました。
よって、算定方式は原価計算方式です。
特に加算はなく、以下の薬価に決定しました。
- セプトカイン配合注カートリッジ1.7mL1管:191.20円
ピーク時の予測販売金額は2.3億円です(予測本剤投与患者数120万人)。
費用対効果評価:ゾコーバ、ベスレミ
中医協総会では、費用対効果評価も行われ、ゾコーバ錠(エンシトレルビル)とベスレミ皮下注(ロペグインターフェロン)の薬価が2025年2月1日から下がります。
- ゾコーバ錠(エンシトレルビル)125mg1 錠:7,407.40 円 → 7,090.00 円
- ベスレミ皮下注(ロペグインターフェロン)250µg0.5mL1 筒:297,259 円 → 272,587 円
- ベスレミ皮下注(ロペグインターフェロン)500µg1mL1 筒:565,154 円 → 518,246 円

なお、糖尿病治療薬のマンジャロ(チルゼパチド)も検討に挙がっていましたが、今回は薬価ダウン無しでした。ホっ…。
-

-
マンジャロ(チルゼパチド)の作用機序、GLP-1受容体作動薬との比較・違い【糖尿病】
続きを見る
あとがき
今回は17製品中、11製品が加算対象でした!多いですね!

また、予測販売金額が100億円を超える新薬は以下の通りでした。
- クービビック錠:199億円
- ユバンシ配合錠:107億円
- ケサンラ点滴静注液:796億円
- テッペーザ点滴静注用:494億円
- アウィクリ注:131億円
新規作用機序を有する薬剤や、利便性が向上している薬剤など、多くの新薬が登場しましたので期待できるのではないでしょうか。
以上、今回は2024年11月20日に薬価収載された新薬17製品についてご紹介しました!
\ 新薬情報オンラインの運営者が執筆! /
薬剤師におススメの記事
失敗しない薬剤師の転職とは?
数多く存在する薬剤師専門の転職エージェントサイト。
どこに登録したらいいのか悩むことも少なくありません。そんな転職をご検討の薬剤師さんに是非見ていただきたい記事を公開しました。
- 新薬情報オンラインの薬剤師2名が実際に利用・取材!
- 各サイトの特徴等を一覧表で分かりやすく掲載!
- 絶対にハズレのない厳選の3サイトを解説!
上手に活用してあなたの希望・条件に沿った【失敗しない転職】を実現していただけると嬉しいです!
-

-
薬剤師の転職サイト3選|評判・求人特徴とエージェントの質を比較
続きを見る

日々の情報収集に最適
-

-
薬剤師の勉強・情報収集に役に立つ無料サイト・ブログ8選
に転職した薬剤師を取材.webp)



























