PASSMED公式LINEの登録者特典|当サイトに掲載している図表の元データ&学習支援AI 薬科GPTをプレゼント♪

2025年9月19日、イミフィンジ(デュルバルマブ)の効能・効果に以下を追加することが承認されました!
- 非小細胞肺がんにおける術前・術後補助療法
- 膀胱がんにおける術前・術後補助療法
アストラゼネカ|ニュースリリース
基本情報
| 製品名 | イミフィンジ点滴静注120mg、同500mg |
| 一般名 | デュルバルマブ(遺伝子組換え) |
| 製品名の由来 | infinity(無限)とimmunotherapy(免疫療法)の頭文字〔IM〕を含む造語 |
| 製造販売 | アストラゼネカ(株) |
| 効能・効果 | 〇切除不能な局所進行の非小細胞肺がんにおける根治的化学放射線療法後の維持療法 〇進展型小細胞肺がん 〇限局型小細胞肺がんにおける根治的化学放射線療法後の維持療法 〇治癒切除不能な胆道がん 〇切除不能な進行・再発の非小細胞肺がん 〇非小細胞肺がんにおける術前・術後補助療法 〇切除不能な肝細胞がん 〇進行・再発の子宮体がん 〇膀胱がんにおける術前・術後補助療法 |
なお、「非小細胞肺がんにおける根治的化学放射線療法後の維持療法」に対する用法・用量は、これまで「2週間間隔」でしたが、2023年11月24日に「4週間間隔」に変更することが承認されました。
イミフィンジは抗PD-L1抗体で免疫チェックポイント阻害薬に分類されています。
2018年7月2日に「切除不能な局所進行の非小細胞肺がんにおける根治的化学放射線療法後の維持療法」を効能・効果として、初めてStageⅢ小細胞肺がんに使用できる免疫チェックポイント阻害薬として登場しました。
その後、以下の適応拡大が行われています。
- 2020年8月21日:進展型小細胞肺がん
- 2022年12月23日:非小細胞肺がん、胆道がん、肝細胞がん
- 2024年11月22日:進行・再発の子宮体がん
- 2025年3月27日:限局型小細胞肺がん
- 2025年9月19日:非小細胞肺がん/膀胱がんにおける術前・術後補助療法

今回は非小細胞肺がん・小細胞肺がん・胆道がん・子宮体がんとイミフィンジ(デュルバルマブ)の作用機序についてご紹介します。
肝細胞がんについては、併用するイジュド(トレメリムマブ)の記事で解説していますので、併せてご参考ください♪
-

-
イジュド(トレメリムマブ)の作用機序【肺がん/肝がん】
続きを見る
非小細胞肺がんと治療について
肺がんは性質や薬の効き方によって“非小細胞肺がん”と“小細胞肺がん”に分類されています。
非小細胞肺がんで発見時に他の臓器に転移がある場合(StageⅣ)は化学療法(抗がん剤や分子標的薬)の治療が中心となります。1)
詳しくは以下の記事をご覧ください。
-

-
イジュド(トレメリムマブ)の作用機序【肺がん/肝がん】
続きを見る
一方、早期に発見できた場合(StageⅠ~Ⅲ)、手術の適応になります。
しかしながら、StageⅢの一部の患者さんでは手術ができない(切除不能)ことがしばしばあり、その場合は白金製剤(シスプラチンやカルボプラチン)を中心とする抗がん剤と放射線治療を併用した治療が行われます。
上記の抗がん剤と放射線治療の併用療法は、通常1~2カ月間行い、その後は無治療で経過観察となります。
しかし経過観察中に多くの患者さんは、がんの進行が認められ、他臓器に転移を引き起こしてしまいます。
今回ご紹介するイミフィンジは本来経過観察を行う期間に投与することで、がんの進行を抑えることが示されていますよ。
また、切除可能なStageⅡA期~ⅢB期において、周術期にイミフィンジを使用(術前は化学療法併用、術後は単剤)することで、再発抑制効果が示されています。
小細胞肺がんと治療について

切除可能な限局型の小細胞肺がんの場合、根治的化学放射線療法が標準ですが、その後は経過観察です。しかしながら、約60%の患者が2年以内に再発すると言われており、予後は不良でした。
イミフィンジは限局型の小細胞肺がんの根治的化学放射線療法に単剤投与することで、再発のリスク低減が期待されています。
続いて、切除不能な小細胞肺がん(進展型小細胞肺がん)の場合、抗がん剤による化学療法が基本です。一次化学療法としては主に以下があります。1)
- シスプラチン+イリノテカン療法
- シスプラチン+エトポシド療法
- カルボプラチン+エトポシド療法
イミフィンジは後述する臨床試験の結果より、カルボプラチン(or シスプラチン)+エトポシド療法と併用して使用することが可能です!
同じく類薬の免疫チェックポイント阻害薬のテセントリク(アテゾリズマブ)はカルボプラチン+エトポシド療法とのみ併用して使用することが可能です。(2019年8月に承認済)
-
-
テセントリク(アテゾリズマブ)の作用機序【肺がん/乳がん/肝がん】
続きを見る
胆道がんとは
肝臓で生成される胆汁(主に脂肪を分解する消化液)は、肝臓内の管を通って十二指腸の乳頭部から放出されます。
この胆汁が通る管のことを「胆管」と呼んでいます。また、胆汁を一時的に貯留する器官が「胆のう」です。

胆道がんはその名の通り、胆道から発生する悪性腫瘍です。
初期にはほぼ無症状ですが、がんが進行すると、
- 黄疸
- 腹痛
- 体重減少、発熱、食欲不振、全身倦怠感
といった症状が発現してきます。2)
治療法
初期に発見できた場合、手術による切除が最も有効な治療になります。
しかし、発見時にがんが大きくて切除できない場合(局所進行)や、他の臓器に転移している場合(遠隔転移)、手術はできません。
この場合、抗がん剤による化学療法が第一選択です。初回治療(一次治療)として使用される化学療法には以下があります。3)

今回ご紹介するイミフィンジはゲムシタビン+シスプラチン療法と併用することで治療効果が認められています!
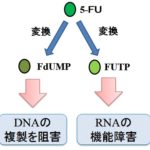
上記の治療に抵抗性・不応となった場合には二次治療が行われますが、残念ながら明確なエビデンスのある治療法がなく、5-FU系抗がん剤(例:S-1等)が選択されることが多いです。3)
-
-
ティーエスワン(TS-1)と5-FUの作用機序と特徴【抗がん剤】
続きを見る
がんの遺伝子検査でMSI-Hと診断された場合にはキイトルーダ(ペムブロリズマブ)が二次治療に行われることもありますね。3)
-
-
キイトルーダ(ペムブロリズマブ)の作用機序【消化器がん/MSI-High固形がん】
続きを見る
FGFR2融合遺伝子が陽性の場合の二次治療としては、ペマジール(ペミガチニブ)が使用できます。
-
-
ペマジール(ペミガチニブ)の作用機序【胆道がん】
続きを見る
子宮体がんと治療
子宮は下部の筒状の「子宮頸部」と、上部の袋状の「子宮体部」に分けられますが、子宮体部から発生するがんを「子宮体がん」と呼んでいます(子宮内膜から発生するので子宮内膜がんとも呼ぶ)。
子宮体がんの治療の基本は手術です。手術後は進行度(ステージ)の決定を行い、再発リスクが高い場合にはプラチナ製剤を含んだ術後補助化学療法が行われることもあります。
また、手術が不可能であったり、全身に転移している場合や、再発した場合には化学療法を行います。
主に使用される化学療法としては、
- パクリタキセル+カルボプラチン(TC療法)
- ドキソルビシン+シスプラチン(AP療法)
などです。
今回、進行・再発の子宮体がんの一次治療として、化学療法(TC療法)単独と比較して、化学療法+イミフィンジ → イミフィンジ+リムパーザ(オラパリブ)によるメンテナンス療法の優位性が認められていますよ。
リムパーザの上乗せは、pMMR例に限る
これまで十数年、ずっと子宮体がんの一次治療はTC療法が主でしたが、ついにそれを上回る治療法が登場です。

-

-
レンビマ(レンバチニブ)の作用機序【肝細胞/甲状腺/子宮体/腎細胞がん】
続きを見る
それではイミフィンジの作用機序に関連する免疫チェックポイントについて解説していきます。
がんと免疫チェックポイント
通常、がんができると生体内の免疫反応が活性化され、がん細胞を死に導こうとしますが、がん細胞はヒトの免疫機構から逃れる術をいくつか持っています。
その一つに、がん細胞ではヒトの免疫反応を抑制する「PD-L1(“ピーディーエルワン”と読みます)」を大量に発現し、免疫反応(T細胞からの攻撃)から逃れています。
PD-L1はT細胞のPD-1(ピーディーワン)と結合することで、T細胞の活性を抑制させる働きがある、いわば、ブレーキのような働きを担っています。
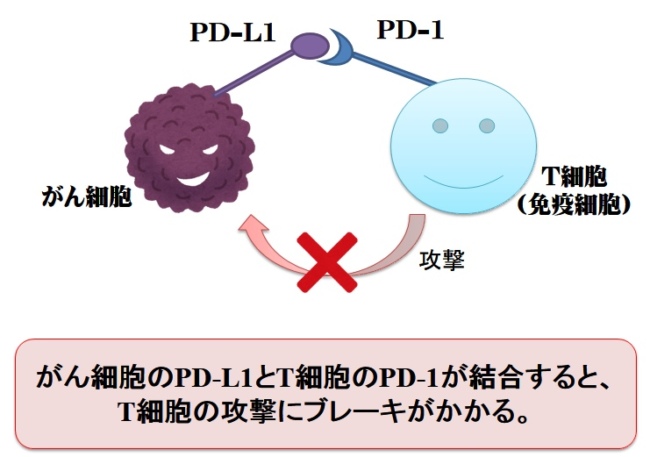
本来、PD-L1やPD-1はT細胞が自己を攻撃しない(自己免疫抑制作用)のために体内に存在していますが、がん細胞はそれを逆手に取っています。
これを“免疫チェックポイント”と呼んでいます。
イミフィンジ(デュルバルマブ)の作用機序
イミフィンジはがん細胞の「PD-L1」を抑制することで、がん細胞のブレーキを解除させ、ヒト本来の免疫反応を活性化させます。
その結果、T細胞が、がん細胞を攻撃することでがん細胞を死に導く、といった作用機序を有しています☆
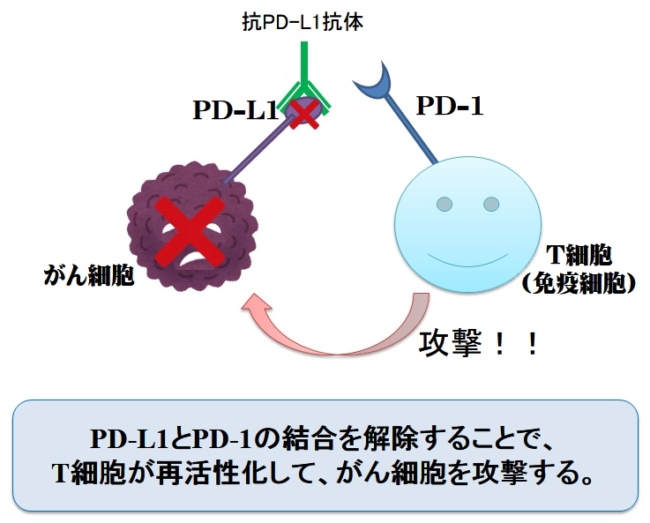
T細胞が活性化され、ヒト本来の免疫力によってがん細胞を攻撃しますので、従来の抗がん剤と比較して副作用が比較的少ないと言われています。
副作用
主な副作用として咳、疲労、肺炎、上気道感染、呼吸困難、発疹、下痢などが報告されています。
また、免疫が過剰になることで自己免疫疾患(例:間質性肺炎、横紋筋融解症、大腸炎、甲状腺機能障害、一型糖尿病、肝炎)等の発現の恐れがあるため、これらの発現には特に注意が必要となります。
非小細胞肺がんのエビデンス:PACIFIC試験
根拠となった臨床試験のPACIFIC試験をご紹介します。4-5)
本試験は白金製剤を用いた根治的同時化学放射線療法の後に進行が認められなかった切除不能局所進行(StageⅢ)の非小細胞肺がん患者さんを対象に、イミフィンジもしくはプラセボを12か月間投与する第Ⅲ相臨床試験です。
主要評価項目は「無増悪生存期間(PFS)」と「全生存期間」で、結果は以下の通りでした。
| 試験名 | PACIFIC試験 | |
| 試験群 | イミフィンジ | プラセボ |
| PFS中央値* | 16.8か月 | 5.6か月 |
| HR=0.52, p<0.001 | ||
| 奏効率† | 28.4% | 16.0% |
| p<0.001 | ||
| 全生存期間中央値 | 未達 | 28.7か月 |
| HR=0.68, p=0.0025 | ||
*無増悪生存期間(PFS):治療を開始してからがんが大きく(増悪)するまでの期間
†奏効率:がんが30%以上縮小した患者さんの割合
このようにイミフィンジ群ではPFS、生存期間を共に延長することが示されています!
ただし、PD-L1の発現率が1%未満の患者さんではイミフィンジの治療効果が弱いことが示唆されています。5)
従って、イミフィンジの最適使用推進ガイドライン6)では以下の記載があります。
PD-L1発現率も確認した上で、本剤の投与可否の判断をすることが望ましい。PD-L1 発現率が1%未満であることが確認された患者においては、本剤の投与の必要性を慎重に判断すること。
小細胞肺がんのエビデンス:CASPIAN試験
小細胞肺がんの根拠となった臨床試験(CASPIAN試験)を紹介します。7)
本試験は進展型の小細胞肺がん患者さんを対象に、一次化学療法として化学療法(カルボプラチンまたはシスプラチン+エトポシド療法)群とそれにイミフィンジを併用する群を比較検討した国際共同第Ⅲ相臨床試験です。
主要評価項目は「全生存期間」で結果は以下の通りでした。
| 試験群 | 化学療法群 | 化学療法+ イミフィンジ群 |
| 全生存期間中央値 | 10.3か月 | 13.0か月 |
| HR=0.73[95%CI 0.59–0.91], p=0.0047 | ||

胆道がんのエビデンス:TOPAZ-1試験
胆道がん一次治療の根拠となった臨床試験(TOPAZ-1試験)を紹介します。8)
本試験は切除不能な胆道がんがん患者さんを対象に、一次化学療法として化学療法(ゲムシタビン+シスプラチン)群とそれにイミフィンジを併用する群を比較検討した国際共同第Ⅲ相臨床試験です(日本を含む)。
主要評価項目は「全生存期間」で結果は以下の通りでした。
| 試験群 | 化学療法群 | 化学療法+ イミフィンジ群 |
| 全生存期間中央値 | 11.5か月 | 12.8か月 |
| HR=0.80[95%CI 0.66-0.97], p=0.021 | ||
胆道がんでも生存期間の有意な延長が認められました!
子宮体がんのエビデンス:DUO-E試験
子宮体がんの一次治療の根拠となった臨床試験(DUO-E試験)をご紹介します。9)
未治療の進行StageIII/IV(FIGO2009)または再発子宮体がん患者さんを対象に、以下の治療群を比較した国際共同第Ⅲ相臨床試験です。
- 対照群:TC療法→プラセボによるメンテナンス(TC群)
- 試験群1: TC療法+イミフィンジ→イミフィンジによるメンテナンス(TC+D群)
- 試験群2:TC療法+イミフィンジ→イミフィンジ+リムパーザによるメンテナンス(TC+D+O群)
本試験の主要評価項目はPFSとされ、結果は以下の通りでした。
| TC群 | TC+D群 | TC+D+O群 | |
| 全集団におけるPFS中央値 | 9.6か月 | 10.2か月 | 15.1か月 |
| - | TC群とのHR=0.71 (0.57-0.89) P=0.003 |
TC群とのHR=0.55 (0.43-0.69) P<0.0001 |
|
| dMMR*におけるPFS中央値 | 7.0か月 | 未到達 | 31.8か月 |
| - | TC群とのHR=0.42 (0.22-0.80) | TC群とのHR=0.41 (0.21-0.75) TC+D群とのHR=0.97 (0.49-1.98) |
|
| pMMR*におけるPFS中央値 | 9.7か月 | 9.9か月 | 15.0か月 |
| TC群とのHR=0.77 (0.60-0.97) | TC群とのHR=0.57 (0.44-0.73) TC+D群とのHR=0.76 (0.59-0.99) |
*dMMRとpMMR:dMMRとpMMRは、DNAミスマッチ修復(MMR)という遺伝子の修復メカニズムに関する用語です。dMMRは、DNAのミスマッチ修復能力が欠如している、または低下している状態を指します。つまり、DNAのコピーエラーや小さな欠陥を修復するメカニズムが正常に働かない状態です。dMMR状態のがんは、特定の免疫療法(例えば、抗PD-1抗体)が効果的であることが示唆されています。一方、pMMRはDNAのミスマッチ修復機能が正常に働いている状態を指します。
全体ではTC群と比較して、TC+D群、TC+D+O群のいずれも有意にPFSを延長しているという結果でした。
サブグループ解析においては、dMMR例に対するリムパーザの上乗せ効果は認められていないようです。
元々、dMMR例は免疫チェックポイント阻害薬の効果が得られやすいので、この集団に対してはイミフィンジの上乗せだけで十分といったところでしょうか。
なお、pMMR例に対してはリムパーザの上乗せ効果が認められているため、国内でもこの集団に対してリムパーザが使用されると考えられますね。
-

-
リムパーザ(オラパリブ)の作用機序【卵巣/乳/膵/前立腺がん】
続きを見る
収載時の薬価
収載時点(2018年8月29日)の薬価は以下の通りです。
- イミフィンジ点滴静注120mg:112,938円
- イミフィンジ点滴静注500mg:458,750円(1日薬価:32,768円)
算定方式等は以下の記事をご覧ください。
-

-
【新薬:薬価収載】9製品(2018年8月29日)と用法用量変化再算定
続きを見る
まとめ・あとがき
イミフィンジはこんな薬
- StageⅢの非小細胞肺がんに使用できる初の免疫チェックポイント阻害薬
- 小細胞肺がんの一次治療として使用可能
- 胆道がんの一次治療として化学療法と併用して使用可能
- 子宮体がんの一次治療として化学療法と併用およびメンテナンスとして使用可能
- がん細胞のPD-L1を抑制することで、がん細胞のブレーキを解除する
StageⅢの非小細胞肺がんでは抗がん剤と放射線治療しか治療選択肢がなく、その後は無治療の経過間観察でした。
抗がん剤と放射線治療による導入療法後にイミフィンジを地固め療法として投与することで、がんの増悪を抑制できるため、新たな治療選択肢として期待されています。

また、胆道がんの一次治療では久しぶりの新薬登場となりました。一次治療で使用可能なゲムシタビン+シスプラチン+S-1療法との使い分けが気になるところですね。
今後は子宮体がんの一次治療でも使用可能のため、予後改善に期待です。
以上、今回は非小細胞肺がん・小細胞肺がん・胆道がん・子宮体がんとイミフィンジ(デュルバルマブ)の作用機序についてご紹介しました。
引用文献・資料等
- 日本肺癌学会|肺癌診療ガイドライン2025年版
- がん情報サービス|胆管がん
- 日本肝胆膵外科学会|胆道癌診療ガイドライン
- PACIFIC試験:N Engl J Med. 2017 Nov 16;377(20):1919-1929.
- PACIFIC試験(追加解析):N Engl J Med. 2018 Dec 13;379(24):2342-2350
- イミフィンジ最適使用推進ガイドライン
- CASPIAN試験:Lancet . 2019 Nov 23;394(10212):1929-1939.
- TOPAZ-1試験:NEJM Evid. 2022 Aug;1(8):EVIDoa2200015.
- DUO-E試験:J Clin Oncol. 2024 Jan 20;42(3):283-299.
\ 新薬情報オンラインの運営者が執筆! /
薬剤師におススメの記事
失敗しない薬剤師の転職とは?
数多く存在する薬剤師専門の転職エージェントサイト。
どこに登録したらいいのか悩むことも少なくありません。そんな転職をご検討の薬剤師さんに是非見ていただきたい記事を公開しました。
- 新薬情報オンラインの薬剤師2名が実際に利用・取材!
- 各サイトの特徴等を一覧表で分かりやすく掲載!
- 絶対にハズレのない厳選の3サイトを解説!
上手に活用してあなたの希望・条件に沿った【失敗しない転職】を実現していただけると嬉しいです!
-

-
薬剤師の転職サイト3選|評判・求人特徴とエージェントの質を比較
続きを見る

日々の情報収集に最適
-

-
薬剤師の勉強・情報収集に役に立つ無料サイト・ブログ8選


































