PASSMED公式LINEの登録者特典|当サイトに掲載している図表の元データ&学習支援AI 薬科GPTをプレゼント♪
2025年6月、ティブソボ錠(イボシデニブ)の「胆道がん」に関する適応拡大が承認申請されました!
日本セルヴィエ|申請のニュースリリース
胆道がんは現時点では未承認です。
基本情報
| 製品名 | ティブソボ錠250mg |
| 一般名 | イボシデニブ |
| 製品名の由来 | 不明 |
| 製造販売 | 日本セルヴィエ(株) |
| 効能・効果 | IDH1遺伝子変異陽性の急性骨髄性白血病 |
| 用法・用量 | アザシチジンとの併用において、通常、 成人にはイボシデニブとして1日1回500mgを経口投与する。 なお、患者の状態により適宜減量する。 |
| 収載時の薬価 | 30,007.60円 |
| 発売日 | 2025年6月2日新発売(HP) |
ティブソボは、2025年3月27日に「IDH1遺伝子変異陽性の急性骨髄性白血病」を対象疾患として承認された国内初のIDH1阻害薬です!
強力な化学療法の適応とならない未治療の急性骨髄性白血病に対して使用されます。

今回は急性骨髄性白血病・胆道がんとティブソボ(イボシデニブ)の作用機序やエビデンスについてご紹介します。
急性骨髄性白血病とは
白血病は「血液のがん」です。
血液細胞には、白血球、赤血球、血小板等がありますが、これら血液細胞の異常化(腫瘍化=がん化)によって引き起こされる病気が白血病です。
また、白血球には
- 顆粒球(骨髄系):好中球、好酸球、好塩基球
- リンパ球(リンパ系):B細胞、T細胞、NK細胞
があります。
急性骨髄性白血病(AML:acute myeloid leukemia)は、白血球の中でも「顆粒球」の未熟細胞が腫瘍化する疾患で、予後は不良とされています。1)
この腫瘍化した未熟な顆粒球のことを「白血病細胞」と呼んでおり、急性骨髄性白血病の約6~10%にIDH1遺伝子変異が認められています。2)
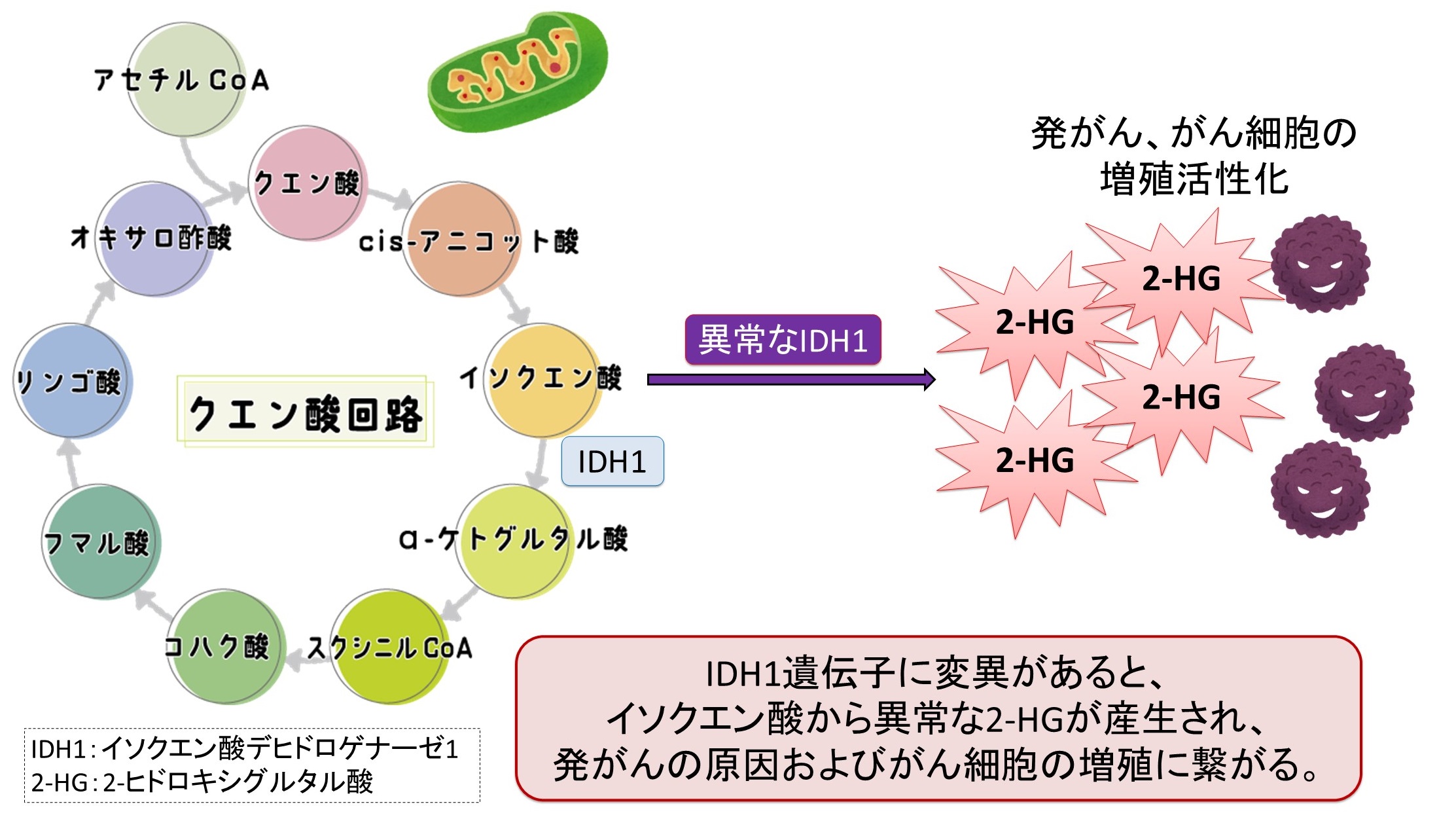

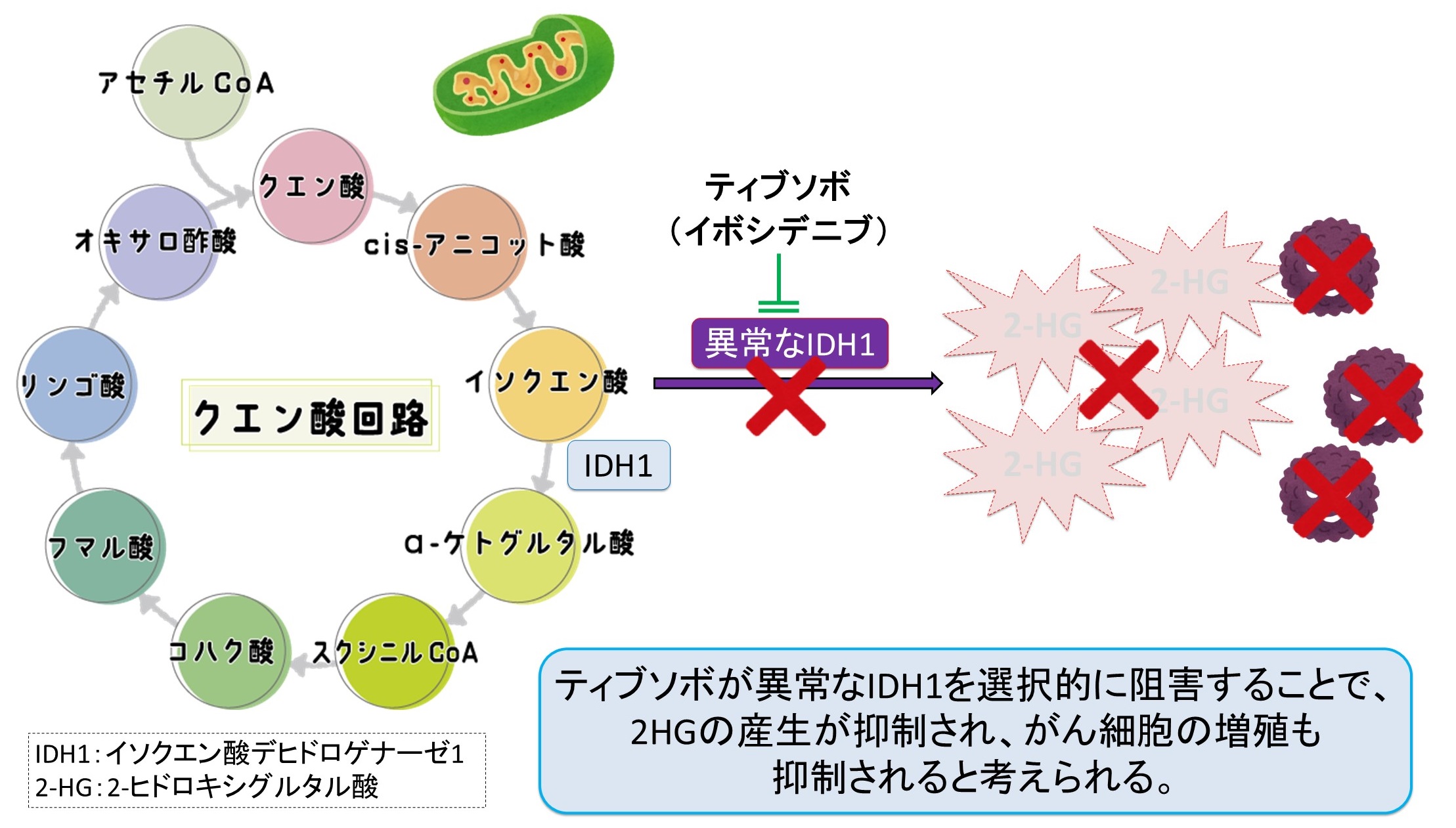
ミトコンドリア内における正常なIDH1は、イソクエン酸をα-ケトグルタル酸に変換していますが、IDH1遺伝子に変異があると、異常なIDH1が産生されます。
この異常なIDH1は、イソクエン酸を2-ヒドロキシグルタル酸(2-HG)に変換してしまい、これが発がんの原因およびがん細胞の増殖に寄与していると考えられています。
予後因子
急性骨髄性白血病には以下のような様々な予後因子が知られています。1)
| 因子 | 予後良好 | 予後不良 |
| 年齢 | 50歳以下 | 60歳以上 |
| 発症様式 | de novo | 二次性 |
| 染色体の核型 | t(8;21) t(15;17) inv(16) or t(16;16) |
3q異常 5・7番の異常 複雑核型 等 |
| 遺伝子異常 | NPM1変異 CEBPA変異 |
FLT3変異 TP53変異 |
| 寛解までの治療期間 | 1回 | 2回以上 |

治療
基本的な治療は、抗がん剤の多剤併用療法(化学療法)です。1)
1カ月程の化学療法(寛解導入療法)によって8割以上の患者さんでは「完全寛解」が得られ、その後、地固め療法を数回行います。
そして完全寛解が5年以上続けば、「治癒」に至ります。
現在、標準的な寛解導入療法は、アントラサイクリン+標準量シタラビンで、具体的には以下のような治療です。
- DNR+AraC療法:ダウノルビシン(DNR)50 mg/m2を5日間+シタラビン(AraC)100mg/m2を7日間持続投与
- IDR+AraC療法:イダルビシン(IDR)12 mg/m2を3日間+シタラビン(AraC)100mg/m2を7日間持続投与
※FLT3変異を有する場合には、上記の寛解導入療法にヴァンフリタ(キザルチニブ)を併用する場合もある
最近では、アントラサイクリン系薬剤のダウノルビシンと、シタラビンを1:5のモル比で配合した新規のリポソーム製剤のビキセオス配合静注用も登場しました。
-
-
ビキセオス配合静注用(ダウノルビシン/シタラビン)の作用機序【AML】
続きを見る
また、標準的な導入化学療法が不適格(例:併存疾患・年齢)な患者さんの初回治療としては、ビダーザ(一般名:アザシチジン)の単剤や、ビダーザ+ベネクレクスタ(ベネトクラクス)が使用されます。
今回ご紹介するティブソボは、標準的な導入化学療法が不適格なAMLの初回治療として、ビダーザと併用で使用します。

胆道がんとは
肝臓で生成される胆汁(主に脂肪を分解する消化液)は、肝臓内の管を通って十二指腸の乳頭部から放出されます。
この胆汁が通る管のことを「胆管」と呼んでいます。また、胆汁を一時的に貯留する器官が「胆のう」です。

胆道がんはその名の通り、胆道から発生する悪性腫瘍です。
初期にはほぼ無症状ですが、がんが進行すると、
- 黄疸
- 腹痛
- 体重減少、発熱、食欲不振、全身倦怠感
といった症状が発現してきます。2)
治療法
初期に発見できた場合、手術による切除が最も有効な治療になります。
しかし、発見時にがんが大きくて切除できない場合(局所進行)や、他の臓器に転移している場合(遠隔転移)、手術はできません。
この場合、抗がん剤による化学療法が第一選択です。初回治療(一次治療)として使用される化学療法には以下があります。3)

最近では一次治療に免疫チェックポイント阻害薬のイミフィンジ(デュルバルマブ)も併用可能になりました。
-

-
イミフィンジ(デュルバルマブ)の作用機序と副作用【肺/胆/肝/子宮体がん】
続きを見る
初回治療を行ったとしてもいずれは抵抗性が生じ、上記治療が不応となってきます。
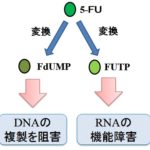
その場合、二次治療が行われますが、残念ながら明確なエビデンスのある治療法がなく、5-FU系抗がん剤(例:S-1等)が選択されることが多いです。3)
-
-
ティーエスワン(TS-1)と5-FUの作用機序と特徴【抗がん剤】
続きを見る
がんの遺伝子検査でMSI-Hと診断された場合にはキイトルーダ(ペムブロリズマブ)が二次治療に行われることもありますね。3)
-
-
キイトルーダ(ペムブロリズマブ)の作用機序【消化器がん/MSI-High固形がん】
続きを見る
今回ご紹介するティブソボはIDH1遺伝子変異が陽性の場合、二次治療として治療効果が期待されている薬剤です!
近年では、FGFR2融合遺伝子陽性が陽性の場合、以下のFGFR阻害薬も使用可能になりましたね。
ティブソボ(イボシデニブ)の作用機序:IDH1阻害薬
ティブソボは、異常なIDH1を選択的に阻害するIDH1阻害薬です。
異常なIDH1が阻害されることで、がん細胞の増殖に寄与していた2-HGの産生が抑制され、がん細胞の増殖抑制効果が得られると考えられますね。
AMLのエビデンス紹介:AGILE試験
根拠となった臨床試験(AGILE試験)をご紹介します。4)
本試験は強力な導入化学療法が適応とならない(例:併存疾患・高齢)未治療のAML患者さんを対象に、ビダーザ(アザシチジン)+プラセボ群と、ビダーザ(アザシチジン)+ティブソボ群を比較する第Ⅲ相臨床試験です。
主要評価項目は「無イベント生存率」とされ、結果は以下の通りでした。
| 試験群 | ビダーザ+ ティブソボ群 |
ビダーザ+ プラセボ群 |
| 12か月時点の 無イベント生存率 |
37% | 12% |
| HR=0.33[95%CI:0.16-0.69], p=0.002 |
||
| 全生存期間中央値 | 24.0か月 | 7.9か月 |
| HR=0.44[95%CI:0.27-0.73], p=0.001 |
||

直接的な比較はできませんが、同様の対象に対して実施されたベネクレクスタの第Ⅲ相臨床試験(VIALE-A試験)5)の結果よりも良好そうな印象を受けます。
胆道がんのエビデンス:ClarIDHy試験
胆道がんの根拠となった臨床試験(ClarIDHy試験)をご紹介します。6)
本試験は、IDH1遺伝子変異陽性で既治療の切除不能・転移性の胆管がん患者さんを対象に、ティブソボ群とプラセボ群を比較した国際共同第Ⅲ相臨床試験です(日本は未参加)。
主要評価項目は「無増悪生存期間(PFS)」とされ、結果は以下の通りでした。
| 試験群 | ティブソボ群 | プラセボ群 |
| PFS中央値 | 2.7か月 | 1.4か月 |
| HR=0·37(95%CI:0.25-0.54) p<0·0001 |
||

副作用
5%以上に認められる副作用として、白血球増加症などが報告されています。
重大な副作用として、
- 分化症候群(11.1%)
- QT間隔延長(16.7%)
- ギラン・バレー症候群(頻度不明)
が挙げられていますので、特に注意が必要です。
分化症候群とは、発熱、皮疹、低酸素症、呼吸機能障害、間質性肺浸潤、胸水・心嚢液貯留等の症状、非感染性の白血球増加症、クレアチニン増加などの症状で、致死的な転帰をたどることがあるとのこと。
用法・用量
アザシチジンとの併用において、通常、成人にはイボシデニブとして1日1回500mgを経口投与します。
なお、患者の状態により適宜減量
収載時の薬価
収載予定時(2025年5月21日)の薬価は以下の通りです。
- ティブソボ錠250mg:30,007.60円(1日薬価:60,015.20円)
算定根拠は以下の記事で解説しています。
-

-
【新薬:薬価収載】10製品(2025年5月21日)
続きを見る
まとめ・あとがき
ティブソボはこんな薬
- 国内初のIDH1阻害薬
- 異常なIDH1を阻害することで2-HGの産生を抑制する
- 分化症候群やQT間隔延長に注意が必要
標準的な導入化学療法が不適格(例:併存疾患・年齢)なAMLに対しては、これまで治療選択肢が限られていました。

ベネクレクスタとの使い分けは今後の検討が待たれるところでしょう。
-

-
ベネクレクスタ(ベネトクラクス)の作用機序と副作用【CLL/AML】
続きを見る
なお、IDH1遺伝子変異は胆道がんでもしばしば認められることから、今回胆道がんでも申請されましたね!今後の適応拡大が待たれるところです。
以上、今回は急性骨髄性白血病・胆道がんとティブソボ(イボシデニブ)の作用機序についてご紹介しました。
引用文献・資料等
- 日本血液学会|造血器腫瘍診療ガイドライン2024年版
- がん情報サービス|胆管がん
- 日本肝胆膵外科学会|胆道癌診療ガイドライン
- AGILE試験(AML):N Engl J Med 2022;386:1519-1531
- VIALE-A試験:N Engl J Med 2020; 383:617-629
- ClarIDHy試験(胆道がん):Lancet Oncol. 2020 Jun;21(6):796-807.
\ 新薬情報オンラインの運営者が執筆! /
薬剤師におススメの記事
失敗しない薬剤師の転職とは?
数多く存在する薬剤師専門の転職エージェントサイト。
どこに登録したらいいのか悩むことも少なくありません。そんな転職をご検討の薬剤師さんに是非見ていただきたい記事を公開しました。
- 新薬情報オンラインの薬剤師2名が実際に利用・取材!
- 各サイトの特徴等を一覧表で分かりやすく掲載!
- 絶対にハズレのない厳選の3サイトを解説!
上手に活用してあなたの希望・条件に沿った【失敗しない転職】を実現していただけると嬉しいです!
-

-
薬剤師の転職サイト3選|評判・求人特徴とエージェントの質を比較
続きを見る

日々の情報収集に最適
-

-
薬剤師の勉強・情報収集に役に立つ無料サイト・ブログ8選


































