★成績優秀者限定の就活|薬学生プレミア
問1 共鳴構造式として誤っているのはどれか。
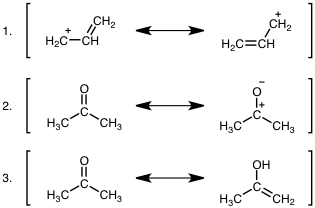
正解は③でした!
【解説】
共鳴構造式では単に電子の位置を変えるだけであって、原子の配置を変えてはいけない。3は平衡式となっている。
問2 オゾン(O3)の構造式として最もふさわしいものを1つ選べ。
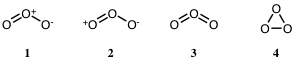
正解は①でした!
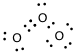
【解説】オゾンのルイス構造式を書くと次のようになる。真ん中の酸素は、もともと持っている電子より一つ少なく、右端の酸素は一つ多くなっている。
問3 以下の元素「S」の酸化数を選べ。
H2SO4
①0
②+2
③+4
④+6
⑤+8
正解は④でした!
【解説】硫黄元素について酸化数を計算すると下記のようになる。
硫黄の酸化数 + 水素の酸化数(+2) + 酸素の酸化数(-8) = 0
したがって、硫黄の酸化数 = +6
問4 下線部の元素の酸化数が+2のものを選べ。
①MnO2
②CuCl
③KMnO4
④[PtCl2(NH3)2]
正解は④でした!
【解説】化合物1-4の下線部の元素について、それぞれ酸化数を計算すると、
①Mn = +4,
②Cu =+1,
③Mn = +7,
④Pt = +2
となる。
問5 酸性が最も強い化合物は次のうちのどれか。1つ選べ。
①CH3CH2OH
②CH3CHO
③CH3COOH
正解は③でした!
【解説】酸性の強さは 3 > 1 > 2の順。化合物2はアルデヒドで水酸基を有さない。化合物1と3では、化合物3の酢酸は共役塩基の負電荷が共鳴安定化によって安定化されるため、化合物1のエタノールよりも酸性度が高い。
問6 塩基性が最も強い化合物は次のうちのどれか。1つ選べ。
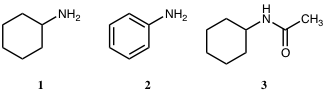
正解は①でした!
【解説】塩基性の強さは 1 > 2 > 3の順。化合物2は非共有電子対が、芳香環上に非局在化するため、塩基性度は低下する。化合物3はアミドで塩基性はない。
問7 ルイス酸は次のうちのどれか。1つ選べ。
①NH3
②AlCl3
③P(C6H5)3
正解は②でした!
【解説】ルイス酸は電子対を受け取ることができる化合物。1,3はルイス塩基。
問8 付加反応は次のうちのどれか。1つ選べ。
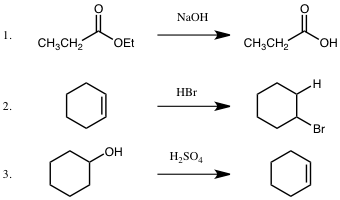
正解は②でした!
【解説】不飽和結合のπ結合が切断される反応が付加反応となるので、反応2が正答となる。反応1は置換反応、反応3は脱離反応。
問9 ラジカル反応は次のうちのどれか。1つ選べ。
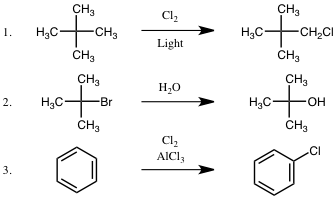
正解は①でした!
【解説】ラジカル反応は光照射で反応が開始する反応1が正解。反応2,3は置換反応。
問10 付加反応は次のうちのどれか。1つ選べ。
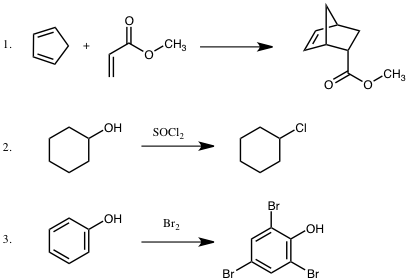
正解は①でした!
【解説】反応1はDiels-Alder反応で、付加環化反応。反応2は置換反応、反応3は求電子置換反応。
成績優秀者ではなくとも就活は有利にできる!








